排序
省局发布《江苏省药品上市后生产场地变更优先受理审评实施细则(试行)》
2024年11月06日,江苏省局发布《江苏省药品上市后生产场地变更优先受理审评实施细则(试行)》(发布之日起实施)。该文件曾在2024年08月05日发布征求意见稿。 文件的目的是加速药品上市后生...
药品上市许可持有人制度的思考- B证的尽头是A证?
1 B证的尽头是A证? 去年10月23日NMPA发布的132号文,对持有人的监管提高了一个新的高度。10月24日药监综药管〔2023〕81号出台的文件其实对各省药监部门监管也提出了很多要求,以强化对持有...
省局答复-纯A证药品生产企业是否可以直接将批文转给另外一家A证企业?
近期收集到朋友向省局老师咨询的答复,与大家分享下。朋友的问题是:“纯A证药品生产企业是否可以直接将批文转给另外一家A证企业?”(注:受让方有相应剂型的生产许可范围) 省局答复如下:...
一张表快速区分检定、校准、计量、标定、校验-附下载资料
检定、校准、计量、标定、校验区别 中文术语英文术语定义目的对象检定Verification查明和确认计量器具是否符合法定要求的程序,它包括检查、加标记和(或)出具检定证书。”会出具检定证书,...
MAH最新监管方向-文献《我国药品上市许可持有人(MAH)制度实施路径问卷调研与结果分析》的思考
今天我们来看一篇发表于《中国食品药品监管杂志》的文献,文献主要内容是由沈阳药科大学亦弘商学院组织开展“我国药品上市许可持有人制度实施路径研究”课题研究。通过对我国MAH 制度落地实施过...
复盘9月份《关于加强药品受托生产监督管理工作的公告(征求意见稿)》意见的函
2024年9月,NMPA流传出一份关于征求《关于加强药品受托生产监督管理工作的公告(征求意见稿)》意见的函(落款时间2024.09.02),这份文件的流出给行业内当时造成了一定的影响。我当时就看完了...
PDA-TR56-阶段适宜性质量体系与药品生产质量管理规范在生物药原液研发中的应用2026修订版-附下载
近日,Parenteral Drug Association(PDA)正式推出《PDA 技术报告第 56 号(修订版):阶段适宜性质量体系与药品生产质量管理规范在生物药原液研发中的应用》(以下简称 TR56 2026 修订版)。...
江苏省局发布《推动企业落实质量安全主体责任的激励和约束措施管理规定》(试行)(征求意见稿)解读
2024年02月23日江苏省局《推动企业落实质量安全主体责任的激励和约束措施管理规定》(试行)(征求意见稿),具体内容大家可以在官网查看,我们主要来分析下这个文件的影响。 此次规定明确了...
工作站的常见几种数据备份的差异
早先写过关于变色龙网络工作站的数据备份,详见Thermo网络工作站(变色龙chromeleon)数据备份。我们知道为了保障数据完整性,制药行业的关键电子数据往往需要进行数据备份,原数据应该在产品生...















kidzhangy6月前0
感谢分享,楼主好人一生平安Terrific7月前0
感谢!特别有用,资源分享的很及时!北岛2年前0
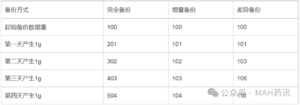
相当于货架期多久?Mark4年前2
Thanks for your blog, nice to read. Do not stop.一位WordPress评论者5年前0
嗨,这是一条评论。 要开始审核、编辑及删除评论,请访问仪表盘的“评论”页面。 评论者头像来自Gravatar。