排序
美国监管部门关于基因与细胞治疗产品的相关法规和指导原则汇总-20220316update
本文主要目的是跟踪美国对于CGT产品法规和指导原则等政策文件,长期更新。 1998.03 Guidance for Industry: Guidance for Human Somatic Cell Therapy GeneTherapy FDA2001.02 Guidance for ...
江苏省局发布药品上市许可持有人药品生产质量安全主体责任清单(2024版)
江苏省局2024年7月份组织的“关于开展企业落实主体责任线上培训”中有提到,省局即将发布的持有人质量安全主体责任正负面清单2024版,替代2023版的清单。 果然08月02日江苏药监发布《关...
欧盟监管部门关于基因与细胞治疗产品的相关法规和指导原则汇总-20220325update
2001.11.06 Directive 2001/83/EC of the European Parliament and of the Council of 6 November 2001 on the Community code relating to medicinal products for human use2005.03 Guideline...
省局发布《江苏省药品上市后生产场地变更优先受理审评实施细则(试行)》
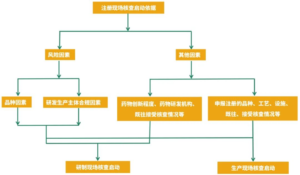
2024年11月06日,江苏省局发布《江苏省药品上市后生产场地变更优先受理审评实施细则(试行)》(发布之日起实施)。该文件曾在2024年08月05日发布征求意见稿。 文件的目的是加速药品上市后生...
加强中药监管?--NMPA发布《中药生产监督管理专门规定》
1. 概述 2024年11月25日,NMPA发布了《中药生产监督管理专门规定(征求意见稿)》。针对中药的日常生产监督提出了具体的要求 2. 主要内容 2.1 &nb...
药品类易制毒化学品的购用证明申请
目前药品类易制毒化学品相关法规中,最重要的就是2010年3月18日发布《药品类易制毒化学品管理办法》(原卫生部令第72号),对于其购用申请按照一般该管理办法中附件6进行。 博主由于公司项目...
解读欧盟GMP附录22征求意见稿:人工智能在药品制造中的应用-附文件下载(双语)
近期,人工智能(AI)正式“入编”欧盟GMP指南! 欧盟引入了全新附录22,为药品及活性物质制造过程中AI的应用设定了明确监管标准。该附录主要关注通过机器学习(ML)实现功能的模型在关键GMP流...
江苏省局发布《推动企业落实质量安全主体责任的激励和约束措施管理规定》(试行)(征求意见稿)解读
2024年02月23日江苏省局《推动企业落实质量安全主体责任的激励和约束措施管理规定》(试行)(征求意见稿),具体内容大家可以在官网查看,我们主要来分析下这个文件的影响。 此次规定明确了...
资源分享-ECA 注射用药品目视检查 V5.0-中英双语
在制药行业,注射用药品的目视检查是保障产品质量与患者安全的关键环节 —— 作为无菌产品放行前的 “最后一道视觉防线”,它直接关系到药品是否存在颗粒污染、容器缺陷等风险。近日,ECA 基金...















kidzhangy6月前0
感谢分享,楼主好人一生平安Terrific7月前0
感谢!特别有用,资源分享的很及时!北岛2年前0
相当于货架期多久?Mark4年前2
Thanks for your blog, nice to read. Do not stop.一位WordPress评论者5年前0
嗨,这是一条评论。 要开始审核、编辑及删除评论,请访问仪表盘的“评论”页面。 评论者头像来自Gravatar。