排序
国内监管部门关于基因与细胞治疗产品的相关法规和指导原则汇总-20230626update
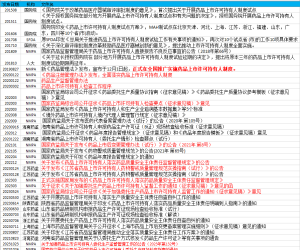
本文主要按照发布时间整理官方关于CAR-T研究的一些法规和技术指导原则,方便查阅相关资料学习。我会持续更新相关内容,如有其他未列出的官方文件,可以留言告诉我,我会持续更新。 1993年-20...
FDA指导原则合集(FDA Guidance Documents)-持续更新
本文持续更新FDA的指导原则并打包,方便离线检索查阅,内容覆盖从FDA发布的从1975至今的所有指导原则,截至2025年7月22日,FDA共发布2275个指南文件。
欧盟监管部门关于基因与细胞治疗产品的相关法规和指导原则汇总-20220325update
2001.11.06 Directive 2001/83/EC of the European Parliament and of the Council of 6 November 2001 on the Community code relating to medicinal products for human use2005.03 Guideline...
装量与规格-江苏省局上市后变更问答的思考
昨天,本公众号发了省局的上市后变更问答(链接:江苏药监-上市后变更专栏近期新增问答汇总)中第三个问题是这样的。 省局贴心地表示该答复来自CDE官网。 确实在CDE通过关键字“增加...
美国监管部门关于基因与细胞治疗产品的相关法规和指导原则汇总-20220316update
本文主要目的是跟踪美国对于CGT产品法规和指导原则等政策文件,长期更新。 1998.03 Guidance for Industry: Guidance for Human Somatic Cell Therapy GeneTherapy FDA2001.02 Guidance for ...
加强中药监管?--NMPA发布《中药生产监督管理专门规定》
1. 概述 2024年11月25日,NMPA发布了《中药生产监督管理专门规定(征求意见稿)》。针对中药的日常生产监督提出了具体的要求 2. 主要内容 2.1 &nb...
麻醉药品和精神药品法规汇总&研发机构如何进行相关药品管理
本文内容涉及麻醉药品和精神药品目前的监管法规汇总,以及对于研发机构如何进行麻醉药品和精神药品的管理两个方面。 1 精神药品相关法规汇总 发布日期机构文件20051101SFDA国家食品药品监...
药品类易制毒化学品的购用证明申请
目前药品类易制毒化学品相关法规中,最重要的就是2010年3月18日发布《药品类易制毒化学品管理办法》(原卫生部令第72号),对于其购用申请按照一般该管理办法中附件6进行。 博主由于公司项目...
江苏省局发布药品上市许可持有人药品生产质量安全主体责任清单(2024版)
江苏省局2024年7月份组织的“关于开展企业落实主体责任线上培训”中有提到,省局即将发布的持有人质量安全主体责任正负面清单2024版,替代2023版的清单。 果然08月02日江苏药监发布《关...

















kidzhangy6月前0
感谢分享,楼主好人一生平安Terrific7月前0
感谢!特别有用,资源分享的很及时!北岛2年前0
相当于货架期多久?Mark4年前2
Thanks for your blog, nice to read. Do not stop.一位WordPress评论者5年前0
嗨,这是一条评论。 要开始审核、编辑及删除评论,请访问仪表盘的“评论”页面。 评论者头像来自Gravatar。