排序
资源分享-CFDI20251015生物制品厂房设施设计与风险控制考虑-厂房设施设计中的无菌保障实践-杨冕
在生物制药行业,厂房设施不仅是生产载体,更是产品质量与安全的 “第一道防线”。尤其是抗体药物、ADC 等生物大分子药物,其生产工艺的复杂性、敏感性对厂房设计提出了极高要求 —— 既要满足 ...
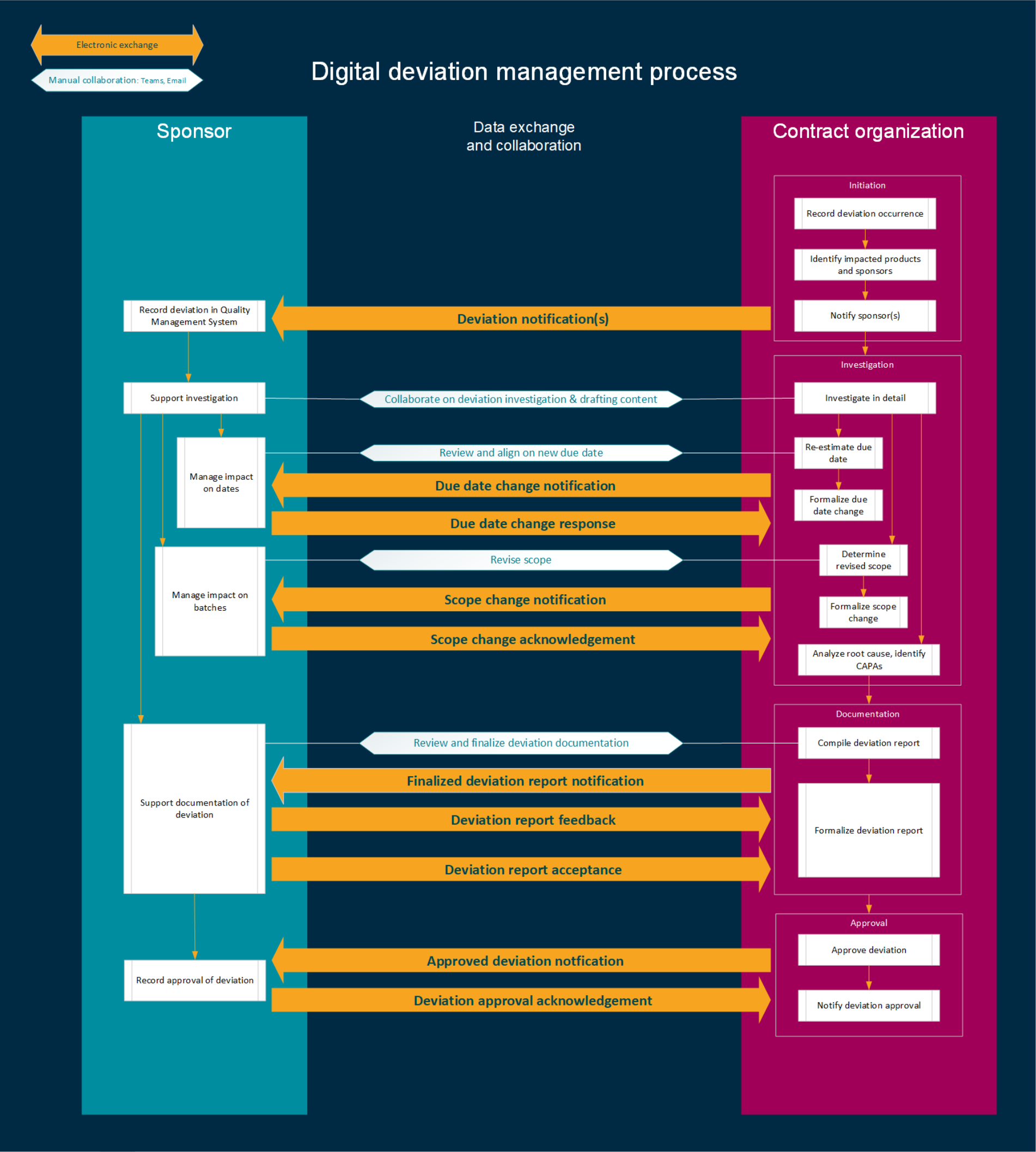
委托生产的数字化偏差管理协同(Digital deviations: Improving sponsor— CMO collaboration-附biophorum双语原文)
摘要 在生物制药行业内管理偏差是确保产品质量、法规合规性以及最终患者安全的关键流程。如今,委托方与合同制造组织(CMOs)之间的偏差管理过程高度依赖人工操作,复杂且分散,导致效率低...
20251209-黑龙江药监问答汇总(药品审评-疫苗-经营-生产检查相关)
药品审评问答 1.《已上市化学药品药学变更研究技术指导原则(试行)》规定,某些中等变更需提供1~3批检验报告,请问具体应该提供几批? 答:指导原则中检验报告批次的设定范围(1~3批)...
资源分享-生物制品质量研究的管理
药品作为特殊商品,其质量直接关系到患者的生命安全与健康。质量研究作为药品研发、生产、流通全链条的核心支撑,是保障药品安全有效的 “生命线”。从质量标准的建立到异常情况的处置,每一个...
资源分享-20251015CFDI生物制品厂房设施设计与风险控制考虑-生物大分子厂房设施设计考虑点-谢一龙
在生物制药行业,厂房设施不仅是生产载体,更是产品质量、生产合规性与运营效率的核心保障。尤其是抗体药物、ADC 药物等生物大分子产品,其生产工艺的复杂性、敏感性对厂房设计提出了极高要求 ...
Public feedback to FDA on regulatory considerations for AI in drug manufacturing(FDA关于AI在药物制造中的监管考虑)-附下载
2025年5月,一篇名为《Public feedback to FDA on regulatory considerations for AI in drug manufacturing》的论文在AAPS Open期刊上发表,由FDA的专家团队撰写。这篇论文总结了公众对FDA 202...
202512-EMA-Shortage Prevention Plan (SPP) and Shortage Mitigation Plan (SMP) pilot report药品短缺预防与缓解试点报告解读-附下载
药品短缺是全球医疗健康领域的重大难题,直接影响患者治疗效果与公共卫生安全。为应对这一挑战,欧盟药品管理局(EMA)联合成员国主管机构(NCAs)推出了药品短缺预防计划(SPP)与短缺缓解计划...
资源分享-从注册核查看临床试验质量管理-广州新药申报服务中心20250926
作为药品上市前的关键监管环节,临床试验质量管理直接关系到受试者权益保护与药品安全有效性评价。近期学习了广州市黄埔区新药申报服务中心李璇老师的《从注册核查看临床试验质量管理》专题分享...
202604-安徽药监-药品委托生产检查常见共性问题
1、委托方机构与人员存在不足: (1)组织架构与职责不清晰,如:质量管理部门的职责缺少指导和监督委托生产过程的内容;未明确企业负责人应定期听取质量管理负责人质量管理工...
资源分享-20251014CFDI药品注册核查工作流程及相关要求总体介绍-杨敬鹏
在医药行业高质量发展的当下,药品注册核查作为保障药品安全性、有效性和质量可控性的关键环节,其重要性愈发凸显。无论是药品研发企业、注册从业者,还是行业监管相关人员,都需要清晰掌握核查...
















kidzhangy6月前0
感谢分享,楼主好人一生平安Terrific7月前0
感谢!特别有用,资源分享的很及时!北岛2年前0
相当于货架期多久?Mark4年前2
Thanks for your blog, nice to read. Do not stop.一位WordPress评论者5年前0
嗨,这是一条评论。 要开始审核、编辑及删除评论,请访问仪表盘的“评论”页面。 评论者头像来自Gravatar。