排序
重磅文献分享-生物制品药学研制核查要点和常见问题分析(2025 CFDI 张平)-附下载
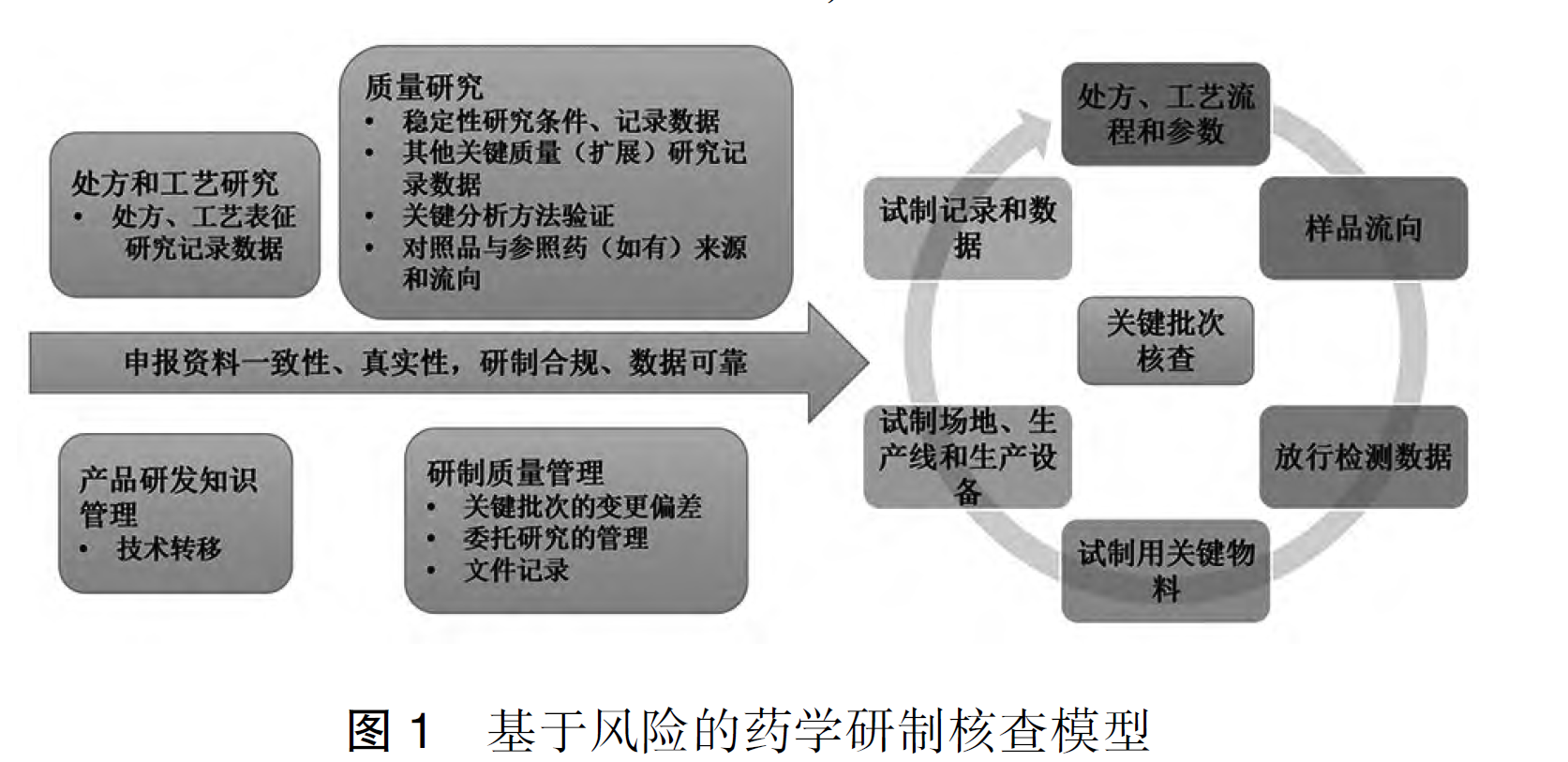
摘要 生物制品的生产和质量控制过程中,存在诸多可变性和特殊性。在新的药品注册监管法规体系下,研制现场核查是促进生物制品研发相关数据真实可追溯,推动生物制品研发行业规范和高质量发展...
书籍分享-GMP Audits in Pharmaceutical and Biotechnology-2024版
《GMP Audits in Pharmaceutical and Biotechnology Industries》系统、全面地阐述了制药与生物技术行业中良好生产规范(GMP)审计的理论框架、实施方法与实际应用,是一本兼具法规高度与实务深...
资源分享-202512-澳门药监局-生物製品生產質量管理規範
文件是澳门特别行政区政府药物监督管理局 2025 年 12 月 12 日发布的第 05/ISAF/2025 号批示,核准了《生物製品生產質量管理規範》(附录 III),并对原有《藥物生產質量管理規範》补充相关特殊...
书籍分享-Process Validation in Manufacturing of Biopharmaceuticals(Third Edition)
《Process Validation in Manufacturing of Biopharmaceuticals(第三版)》聚焦生物制药生产过程验证的核心需求,系统涵盖 FDA 2011 年工艺验证指南解读、风险评估(如 FMEA)、工艺表征、缩小...
202510-ISPE-Novel Technology Applied to Biologics Manufacturing新技术赋能生物制品生产-附下载
2025 年 10 月 26-29 日,2025 ISPE 年会在美国夏洛特市举办并同步开放虚拟参会,复宏汉霖总裁魏东以《Novel Technology Applied to Biologics Manufacturing》为题,分享了生物制造行业趋势、...
202512FDA指南-Promotional Labeling and Advertising Considerations for Prescription Biological Reference Products, Biosimilar Products, and Interchangeable Biosimilar Products Questions and Answers 生物类似药促销宣传的合规指南问答-附下载
2025 年 12 月,美国食品药品监督管理局(FDA)发布了《处方药生物参考产品、生物类似药和可互换生物类似药的促销标签和广告考量问答指南》,为制药企业的合规宣传提供了明确指引。在生物类似药...
资源分享-病毒性疫苗研发:如何做好进度和质量的平衡
“在资本、监管、竞争的三重高压下,如何既跑出速度、又守住质量底线、不在核查时翻车?”课件以第01章“疫苗研发项目管理”开篇,直击行业现状与痛点(进度永远赶不上老板预期、质量永远被进度...
资源分享-生物制品基于药品生命周期观的系统设计
药品生命周期绝不仅仅是从研发到退市的“时间轴”,更是一条必须用系统化研究和全方位管理串起来的“质量链”,早期任何设计缺陷,后期放大成本都会呈指数级上升,因此从临床前就要按ICH Q8/Q10...
资源分享-生物制品工艺研发的管理
这是一份生物制品(疫苗)工艺研发全流程风险管控干货课件,核心贯穿ICH Q8“质量源于设计(QbD)”理念,强调从小试到商业化全程用风险评估、数据积累、异常闭环来构建稳健工艺,确保工艺可重...
资源分享-生物制品安评批和临床申报批制备的管理
这是一份极其实战的生物制品(疫苗)IND药学开发指南,核心贯穿“关键批次(安评批+IND注册批)必须100%真实、可追溯、风险前控、QbD全程驱动”这一条主线。课件从法规要求入手,引用30号文、IC...




















kidzhangy5月前0
感谢分享,楼主好人一生平安Terrific6月前0
感谢!特别有用,资源分享的很及时!北岛2年前0
相当于货架期多久?Mark4年前2
Thanks for your blog, nice to read. Do not stop.一位WordPress评论者5年前0
嗨,这是一条评论。 要开始审核、编辑及删除评论,请访问仪表盘的“评论”页面。 评论者头像来自Gravatar。