排序
资源分享-DB13/T5482-2022《药品不良反应快速报告导则》
DB13/T5482-2022《药品不良反应快速报告导则》由河北药监于 2022 年 2 月 28 日发布、3 月 31 日实施,适用于药品上市许可持有人的上市后药品不良反应快速报告工作(不适用于疫苗疑似预防接种异...
从昆明制药WHO检查报告看API企业的国际化合规道路-附下载
近期,世界卫生组织(WHO)发布了针对昆明制药集团股份有限公司(KPC Pharmaceuticals, Inc.)的公开检查报告(WHOPIR)。此次审计于2025年6月9日至13日进行,旨在对其生产的原料药(API)蒿甲...
202510-MHRA-Decentralised Manufacturing-overview and considerations去中心化制造概况和考虑-附下载
2025 年 10 月,在夏洛特举办的 ISPE 年会上,英国药品和医疗保健产品监管局(MHRA)重磅解读了全新的分散制造(Decentralised Manufacturing, DM)监管框架。这一框架的落地不仅是制药行业监管...
资源分享-T/SHPPA 010-2025《药品生产数字化质量保证技术要求》
技术要求的亮点剖析 文件的主体是第4章“技术要求”,分为多个子部分。这里我用表格总结一下,便于大家对比和理解: 子部分主要内容亮点与影响4.1 DQA构建基本要求可访问性、可追溯性、可...
资源分享-临床前动物安评的管理(法规要求和注意事项)
文件从法规、实操、合作管理三个维度,聊聊临床前动物安评的那些关键要点。 链接:https://pan.quark.cn/s/7661c7f29ec8
202512-加拿大司法部-Controlled Drugs and Substances Act受管控药物和活性物质法案-附下载
《受管控药物和活性物质法案》核心是规范受管制物质(附表 I-V)、前体(附表 VI)及相关设备(附表 IX)的生产、贩卖、进出口、持有等行为,明确了各类罪名及分级处罚(含终身监禁至短期监禁、...
资源分享-20251014CFDI药品注册核查工作流程及相关要求总体介绍-杨敬鹏
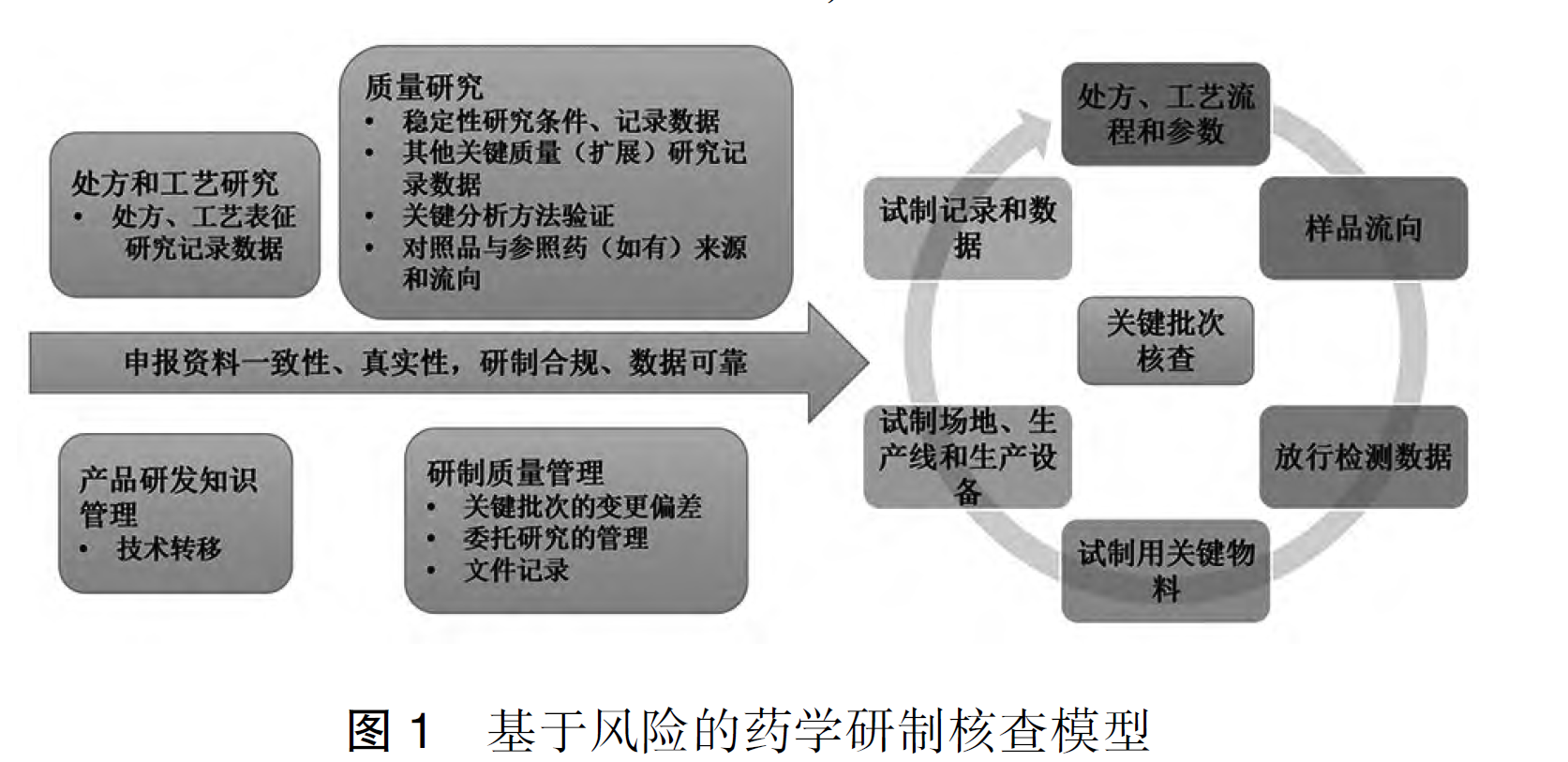
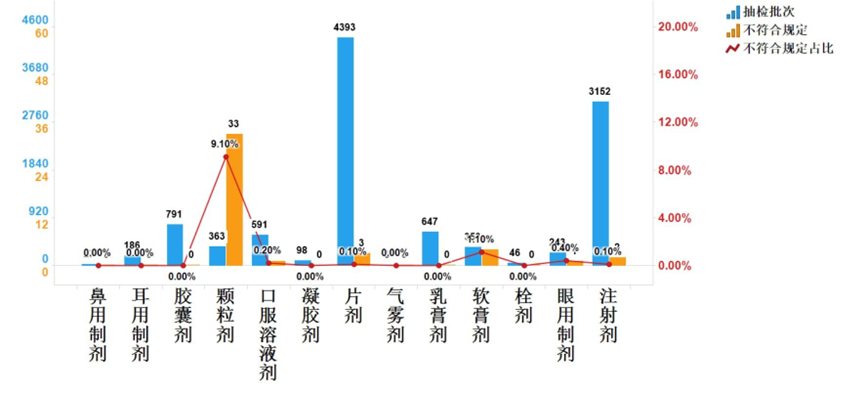
在医药行业高质量发展的当下,药品注册核查作为保障药品安全性、有效性和质量可控性的关键环节,其重要性愈发凸显。无论是药品研发企业、注册从业者,还是行业监管相关人员,都需要清晰掌握核查...
资源分享-2019-中检院-食品检验操作技术规范(理化检验)
《食品检验操作技术规范(理化检验)》是《中国食品药品检验检测技术系列丛书》的重要组成部分,由中国食品药品检定研究院组织长期从事食品检验检测的业务骨干编写,全书分为食品检验通则、食品...
资源分享-202512-加拿大卫生部HC-Draft Guidance Document for Clinical Trial Sponsors: SGBA Plus Demographics Action Plan in Clinical Trial Applications临床试验申办者指导文件草案:临床试验申请中 SGBA 扩展版人群特征行动计划
这份 2025 年 12 月加拿大卫生部发布的指南草案,面向开展或计划开展药物临床试验的申办者,核心是就自愿提交的 SGBA Plus(性别及交叉人口统计因素分析)人口统计行动计划(DAP)提供指导,虽...
资源分享-202501消毒剂相关培训
文件为消毒剂相关培训资料,核心围绕消毒剂作用原理与效果确认两大模块展开。在作用原理部分,明确了消毒、灭菌、无菌等关键定义,按氧化类、酚类、醛类、醇类等类别详解其杀菌机理、特点及适用...

















kidzhangy4月前0
感谢分享,楼主好人一生平安Terrific5月前0
感谢!特别有用,资源分享的很及时!北岛2年前0
相当于货架期多久?Mark4年前2
Thanks for your blog, nice to read. Do not stop.一位WordPress评论者5年前0
嗨,这是一条评论。 要开始审核、编辑及删除评论,请访问仪表盘的“评论”页面。 评论者头像来自Gravatar。