排序
重磅文献分享-生物制品药学研制核查要点和常见问题分析(2025 CFDI 张平)-附下载
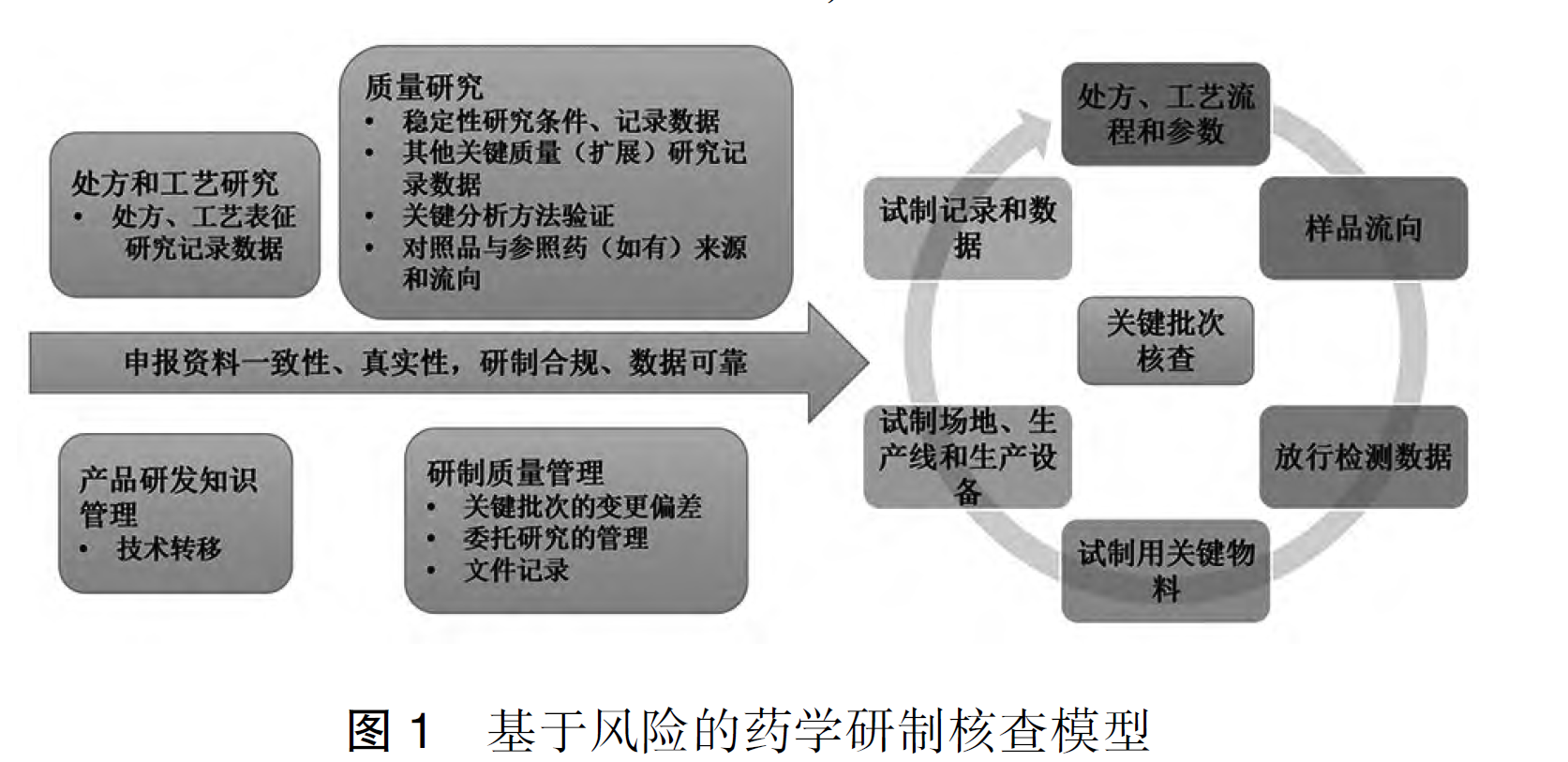
摘要 生物制品的生产和质量控制过程中,存在诸多可变性和特殊性。在新的药品注册监管法规体系下,研制现场核查是促进生物制品研发相关数据真实可追溯,推动生物制品研发行业规范和高质量发展...
海南药监-关于药品变更相关问题的百问百答-附下载
全文下载链接:https://pan.quark.cn/s/edac9bc8417e 第一篇 申报流程 问题 1:药品备案类变更受理形式审查及技术审查流程是什么? 答:1. 申请人提交申请申请人按照《国家药...
文献解读-抗体偶联药物生产关键环节GMP检查研究(2025CFDI官方文献)-附下载
在肿瘤治疗进入精准医疗的今天,抗体偶联药物(ADC)凭借 “单克隆抗体的靶向性 + 小分子毒素的强杀伤性” 的独特优势,成为生物医药领域的 “明星赛道”。这种被称为 “生物导弹” 的新型药物...
资源分享-CMDE-中国医疗器械器审中心答疑解惑汇总(202511)
医疗器械器审中心发布的 6.3 版答疑解惑汇总(2025 年 11 月 17 日),收录了 2017 年至 2025 年间的 530 个核心问题及解答,聚焦医疗器械与体外诊断试剂注册申报、临床评价、检测验证、技术要...
ASTM E2656-25 标准实践——制药用水中总有机碳(TOC)属性的实时释放测试指南(Standard Practice for Real-time Release Testing of Pharmaceutical Water for the Total Organic Carbon Attribute)-附下载地址
在药品和生物制药制造中,水是使用最广泛的成分或原料。其纯度,特别是总有机碳(TOC)含量,直接关系到最终产品的质量。传统上,我们依赖于实验室取样和分析的模式进行水质放行,这种模式耗时...
资源分享-2025年医药行业年终总结-政策篇(易联招采网)
这份 文件是《2025 年医药行业年终总结政策篇》(236张幻灯片),主要内容是对 2025 年医药行业政策环境的全面总结和分析。 PPT 涵盖了医药行业的多个重要政策领域:从医药卫生体制改革、药...
解读 WHO 2026 版医药产品技术新规:供应商合规与质量保障指南Technical Requirements for Medicines and Health products In ITBs/RFQs-附下载
2026 年 1 月,世界卫生组织(WHO)发布了《招标 / 询价中药品和健康产品技术要求》(第 5 版),旨在通过更严格、更细致的技术规范,保障全球范围内 WHO 采购产品的质量、安全性和可及性。这份...
20260320-EMA-Chemistry of active substances (chemistry of new active substances)活性物质的化学指南-附下载
欧盟药品管理局(EMA)于2026年2月16日正式采纳并发布了修订版《活性物质的化学指南》(Guideline on the chemistry of active substances,EMA/CHMP/QWP/49484/2026),该指南将于2026年9月1日...
值得参考-广东药监发布关于进一步加强药品委托生产监督管理的通知
7月12日,为了进一步加强药品委托生产监督管理,广东省发布了相关事项的通知,对B证持有人及受托生产企业上市后的监督管理工作提出了一些要求。
ECA-审计追踪审查通用SOP征求意见稿2025-附下载
本文件基于风险评估,提供了一个清晰的框架,帮助制药企业确保患者安全和产品质量。下面,我将解读这份文件的要点,并结合实际应用分享我的见解。 文件概述 指导GMP计算机化系统的审计轨...

















kidzhangy6月前0
感谢分享,楼主好人一生平安Terrific7月前0
感谢!特别有用,资源分享的很及时!北岛2年前0
相当于货架期多久?Mark4年前2
Thanks for your blog, nice to read. Do not stop.一位WordPress评论者5年前0
嗨,这是一条评论。 要开始审核、编辑及删除评论,请访问仪表盘的“评论”页面。 评论者头像来自Gravatar。