排序
202512-EMA-Guideline on the Development and Manufacture ofSynthetic Peptides-合成肽的开发与生产指南-附下载
该文件是欧洲药品管理局(EMA)于 2025 年 12 月发布的《合成肽的开发与生产指南》(2026 年 6 月生效),旨在规范合成肽类药物的开发、生产、表征、质量控制等关键环节,补充现有相关指南未覆...
一文读懂 EDQM CEP 申请与变更批准全流程-Stepwise process to get a CEP/having a change approved-附下载
对于制药企业而言,获得欧洲药典适用性证书(CEP)是产品进入欧洲及全球多个国家市场的核心门槛之一。欧洲药品质量管理局(EDQM)2025年10月最新发布的《CEP 申请及变更批准分步流程》(PA/PH/C...
FDA 7346.832M 全解读:2026 生物制品 GMP & 数据完整性检查-附双语版下载
2026 年 4 月,FDA 正式发布7346.832M 合规计划,并于5 月 14 日全面实施。这份长达 83 页的指南,是 CDER 针对蛋白类生物制品生产商的上市前许可检查 (PLI)与批准前检查 (PAI) 的核心依据,直...
202509-EMA-Guidelines on the details of the various categories of variation欧盟药品上市许可变更新指南(2026生效)-附下载
2026 年 1 月 15 日,欧盟《药品上市许可变更分类及流程指南》(C/2025/5045)将正式生效,替代沿用 13 年的 2013 版指南。这份经 2024 年修订的新规,通过简化流程、优化分类、强化工作共享机...
转载-2025年CDE官方问答全梳理(截至20260109)
2025年,国家药品监督管理局药品审评中心(CDE)持续围绕药品注册申报中的关键环节、高频疑问与共性难题,发布了一系列具有指导意义的共性问题解答。为帮助业界更清晰把握政策导向、提升申报效...
202512-广东药监-广东省药品审评检查沟通咨询问答500问-附下载
广东省药品审评检查沟通咨询问答500问,下载链接:https://pan.quark.cn/s/55172853f56c 第一篇 生物制品、麻醉药品、精神药品、医疗用毒性药品、药品类易制毒化学品、放射性药品...
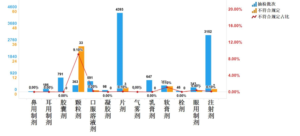
国家药品抽检年报(2023)解读
2024年3月26日,中检院发布了《国家药品抽检年报(2023)》,报告中展示了2023年我国药品抽检工作取得了成果。报告中显示, 2023年共完成了132个品种18762批次制剂产品与中药饮片的抽检任务,涉...
资源分享-Container Closure Integrity Testing of Medicinal Products for Parenteral Use(ECA发布注射用药品容器密封完整性测试立场文件第三版-202511)
注射用药品因直接进入人体循环系统,其包装密封完整性(Container Closure Integrity, CCI)直接关系到产品无菌性、药效稳定性及患者用药安全。 ECA发布的《注射用药品容器密封完整性测试立场文...
药审云课堂答疑汇总(2024年12月-2025年12月)-转自iReg
问题1:起始原料引入两个手性碳,可能存在4个异构体,并且起始原料无紫外吸收,异构体研究难度较大,不在起始原料中进行控制,在中间体及成品中研究是否可行? 解答1:首先建议参考ICH Q11及...
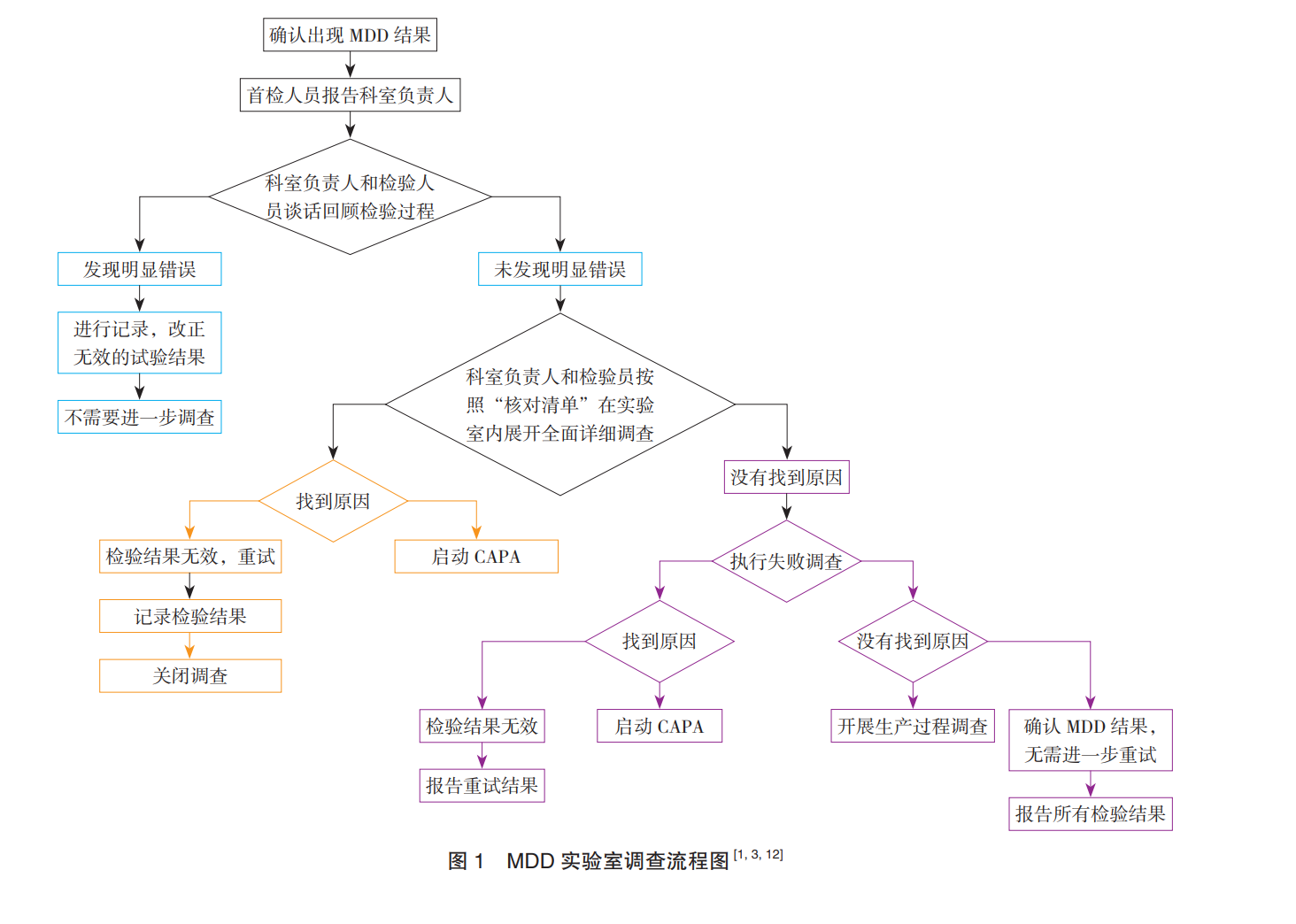
重磅文献分享-药品微生物数据偏差调查规范和研究概述-文末附下载地址
偏差是指使结果与事实之间存在差异的系统性倾向,数据的来源、数据处理方式等都可能导致偏差。微生物数据偏差(Microbial Data Deviation,MDD)于 2001 年由美国食品药品管理局(Food and ...














kidzhangy6月前0
感谢分享,楼主好人一生平安Terrific7月前0
感谢!特别有用,资源分享的很及时!北岛2年前0
相当于货架期多久?Mark4年前2
Thanks for your blog, nice to read. Do not stop.一位WordPress评论者5年前0
嗨,这是一条评论。 要开始审核、编辑及删除评论,请访问仪表盘的“评论”页面。 评论者头像来自Gravatar。