排序
资源分享-药用辅料和药品包装材料检验技术2019版
药用辅料和药品包装材料检验技术》是一本集理论性、实用性和权威性于一体的专业技术书籍。它不仅为药品检验工作提供了系统的技术指导,也为药品质量保证体系建设提供了重要支撑。在当前药品监管...
批判性思维,而非简单分类——深度解读Waters 白皮书《Critical Thinking, Not Categorization》-附下载地址
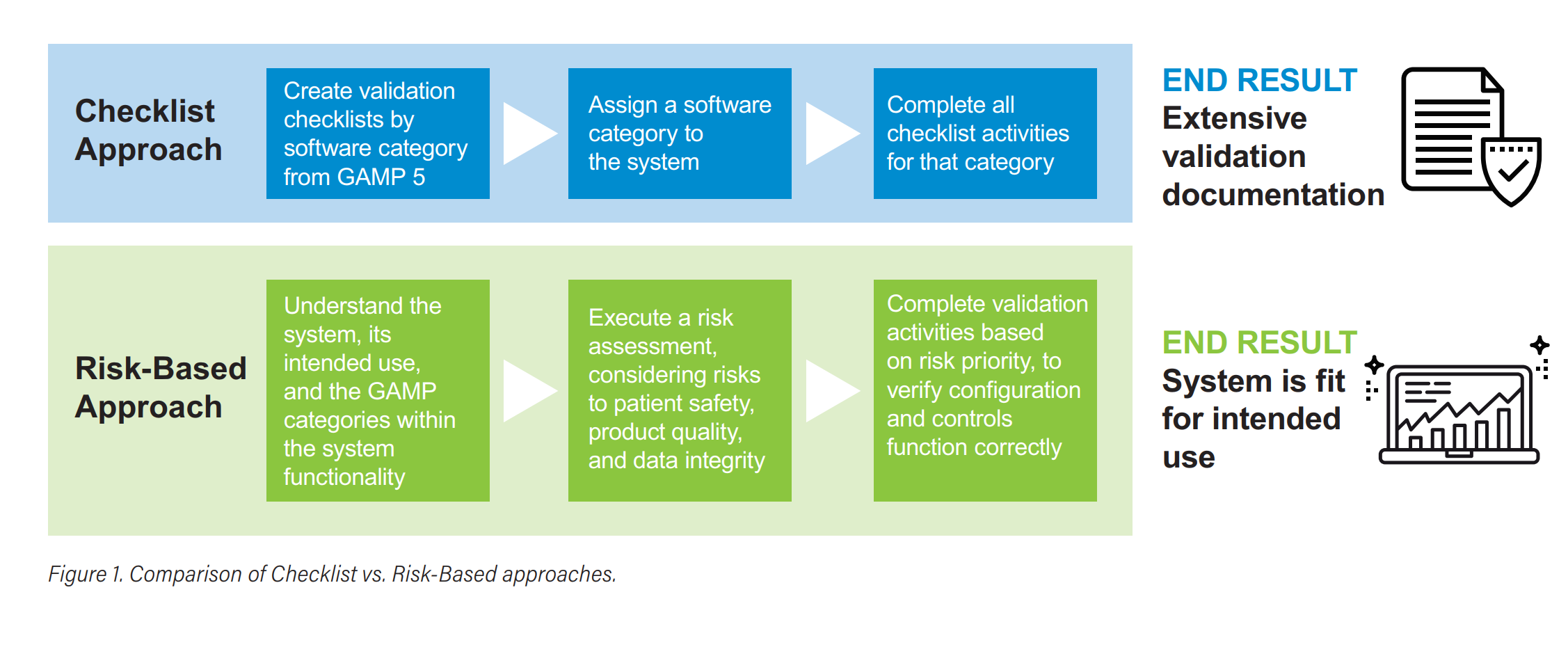
在制药合规圈子里,提到计算机化系统验证(CSV),很多人第一反应就是“这个系统是GAMP几类?我按类别走文档和测试清单就行了”。 但如果你还这么想,真的该好好读读Waters这篇2021年的白皮书了...
202511-PDA-从极端污染控制失败中吸取教训Contamination Control Failures-What we learn from worst case scenarios-附下载
在生物制药行业,无菌生产是不可逾越的红线,而污染控制则是守护这条红线的核心防线。然而,即使是流程规范的药企,也可能因看似微小的疏忽陷入污染危机。近日,Parenteral Drug Association(P...
202510-MHRA-Decentralised Manufacturing-overview and considerations去中心化制造概况和考虑-附下载
2025 年 10 月,在夏洛特举办的 ISPE 年会上,英国药品和医疗保健产品监管局(MHRA)重磅解读了全新的分散制造(Decentralised Manufacturing, DM)监管框架。这一框架的落地不仅是制药行业监管...
资源分享-202509-浙江市场监督-人工智能企业商业秘密保护指引
浙江省市场监督管理局 2025 年 9 月发布的《人工智能企业商业秘密保护指引》,依据相关法律法规,作为 2020 年《商业秘密保护工作指引》的分指引,针对人工智能企业在算法、模型、数据等核心商...
药审云课堂答疑汇总(2024年12月-2025年12月)-转自iReg
问题1:起始原料引入两个手性碳,可能存在4个异构体,并且起始原料无紫外吸收,异构体研究难度较大,不在起始原料中进行控制,在中间体及成品中研究是否可行? 解答1:首先建议参考ICH Q11及...
海南药监-关于药品变更相关问题的百问百答-附下载
全文下载链接:https://pan.quark.cn/s/edac9bc8417e 第一篇 申报流程 问题 1:药品备案类变更受理形式审查及技术审查流程是什么? 答:1. 申请人提交申请申请人按照《国家药...
资源分享-20251014CFDI药品注册核查工作流程及相关要求总体介绍-杨敬鹏
在医药行业高质量发展的当下,药品注册核查作为保障药品安全性、有效性和质量可控性的关键环节,其重要性愈发凸显。无论是药品研发企业、注册从业者,还是行业监管相关人员,都需要清晰掌握核查...
资源分享-PDA TR88 Microbial Data Deviation Investigations in the Pharmaceutical Industry制药行业中的微生物偏差调查中英文双语及思维导图
PDA 发布的TR 88《制药行业微生物数据偏差调查》,旨在弥补 FDA 相关指南在微生物偏差调查方面的不足,提供行业最佳实践。报告定义微生物数据偏差为超出药品注册申请、GMP 法规等设定标准的微生...
书籍推荐-《The ASQ Certified Quality Engineer Handbook》(ASQ 认证质量工程师手册)第五版
本书是《The ASQ Certified Quality Engineer Handbook》(ASQ 认证质量工程师手册)的第五版,由 Scott A. Laman 编辑,出版于 2022 年,由 ASQExcellence 发行。全书总页数超过 576 页(从目...




















kidzhangy5月前0
感谢分享,楼主好人一生平安Terrific6月前0
感谢!特别有用,资源分享的很及时!北岛2年前0
相当于货架期多久?Mark4年前2
Thanks for your blog, nice to read. Do not stop.一位WordPress评论者5年前0
嗨,这是一条评论。 要开始审核、编辑及删除评论,请访问仪表盘的“评论”页面。 评论者头像来自Gravatar。