排序
IT基础设施控制与合规性:制药行业GxP指南解析
今天,我想和大家分享一份关于IT基础设施控制和合规性的笔记文档分析。这份文档名为202512《IT基础设施控制和符合性笔记》,总共48页,主要针对制药行业的GxP法规环境,提供了一种结构化的方法...
资源分享-生物制品安评批和临床申报批制备的管理
这是一份极其实战的生物制品(疫苗)IND药学开发指南,核心贯穿“关键批次(安评批+IND注册批)必须100%真实、可追溯、风险前控、QbD全程驱动”这一条主线。课件从法规要求入手,引用30号文、IC...
资源分享-上海合成生物与生物制造产业发展白皮书(2025)
《上海合成生物与生物制造产业发展白皮书(2025)》由上海市合成生物产业协会与沙利文联合发布,系统阐述了合成生物学作为第三次生命科学革命和新质生产力的核心价值,梳理了其与生物制造 “从 ...
书籍分享-GMP计算机化系统实施与检查指南(2025版张金贵)
《GMP 计算机化系统实施与检查指南》由张金贵所著,聚焦药品生产领域计算机化系统的 GMP 合规管理,系统涵盖计算机化系统的定义、分类、GMP 基本要求与管理框架,详细阐述系统开发与验证、运行...
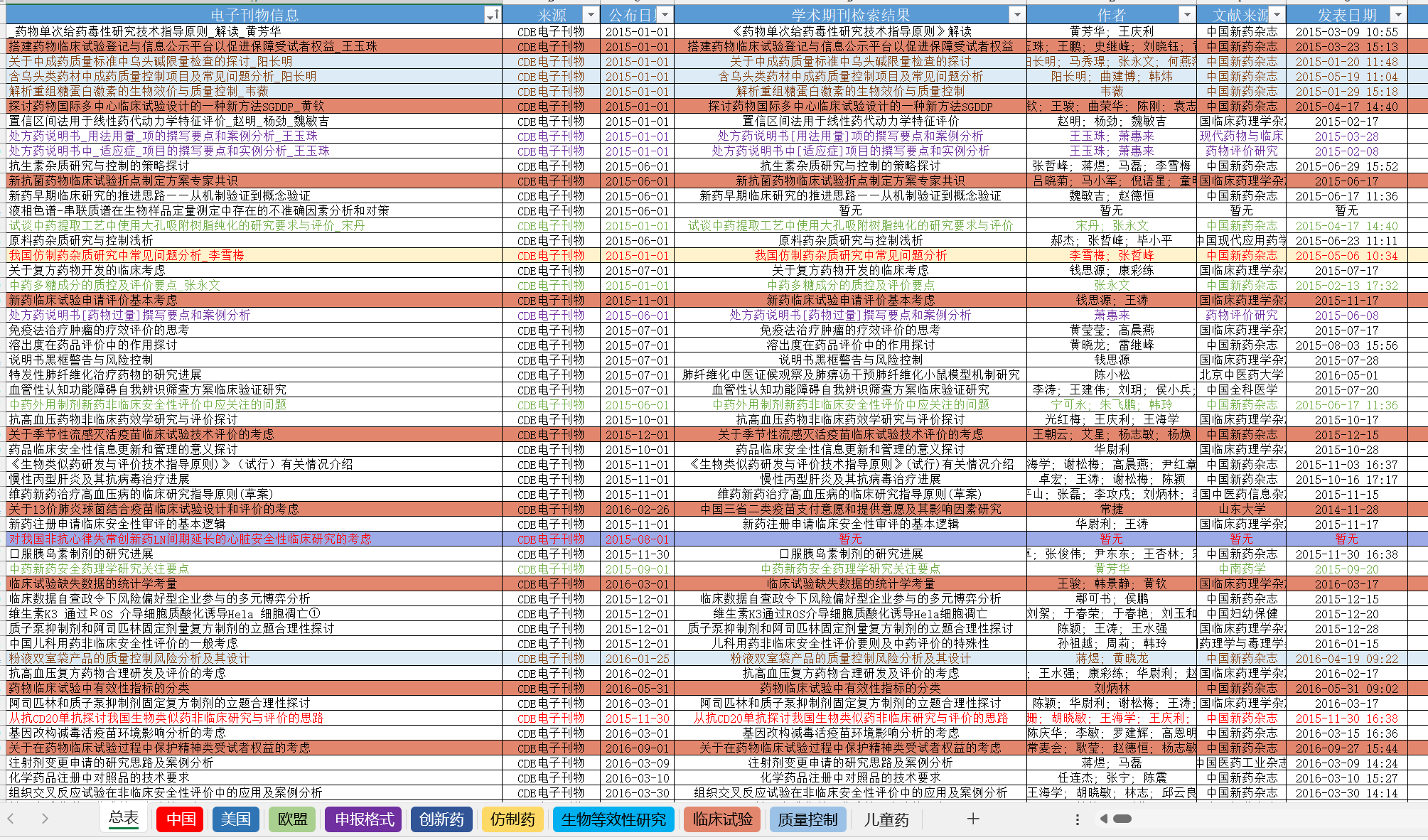
资源分享-CDE电子刊物总览
引言 在药品研发、审评和监管领域,及时获取专业、全面的信息至关重要。今天要给大家分享一份资源 ——CDE 电子刊物总览(2015-至今),这是一个涵盖丰富药品领域知识的信息宝库。 内...
重磅资料分享-药品生产场地变更汇总国家局及各省局
允咨医药培训中心对国家局及各省局药品生产场地变更相关问答与实施细则进行汇总,内容涵盖变更分类(重大、中等、微小变更)、不同场景(省内 / 省外委托生产、企业内部车间变更、长期未生产恢...
资源分享-20251217-以数据完整性为中心的分析仪器确认和计算机化系统验证思维导图
该思维导图围绕以数据完整性为核心的分析仪器确认与计算机化系统验证展开,聚焦 USP<1058> 标准,涵盖其修订背景、主要变化(如允许合并文档)及对 IQ、OQ、PQ 理解与执行的影响,同时结合 G...
资源分享-202512-EMA-Guideline on stability testing for applications for variations to a marketing authorisation(EMA 稳定性试验变更指南)
2025 年 12 月,欧洲药品管理局(EMA)发布了修订后的《上市许可变更申请稳定性试验指南》(EMA/CHMP/QWP/441071/2011-Rev.3),该指南将于 2026 年 1 月 15 日正式生效,全面替代 2011 年版 Re...
2025-EMA-HUMAN MEDICINES IN 2025 (2025人用药物年度报告)-附下载
2025 年,欧洲药品管理局(EMA)交出了一份亮眼的药品监管与创新成绩单。从 104 个新药积极授权意见到罕见病治疗的突破性进展,从生物类似药的爆发式增长到全球公共卫生的跨区域协作,这一年的...
资源分享-浙江省药品检查中心《药品生产企业药用辅料和包材常见缺陷分析》(2025.09.19)-附下载
在当前的药品生产监管环境下,“物料系统”(特别是辅料和包材)正成为飞行检查和注册核查的重灾区。很多企业往往重原料药、轻辅料包材,导致在合规性上频频“踩雷”。朱老师关于《药品生产企业...

















kidzhangy6月前0
感谢分享,楼主好人一生平安Terrific7月前0
感谢!特别有用,资源分享的很及时!北岛2年前0
相当于货架期多久?Mark4年前2
Thanks for your blog, nice to read. Do not stop.一位WordPress评论者5年前0
嗨,这是一条评论。 要开始审核、编辑及删除评论,请访问仪表盘的“评论”页面。 评论者头像来自Gravatar。