排序
复盘9月份《关于加强药品受托生产监督管理工作的公告(征求意见稿)》意见的函
2024年9月,NMPA流传出一份关于征求《关于加强药品受托生产监督管理工作的公告(征求意见稿)》意见的函(落款时间2024.09.02),这份文件的流出给行业内当时造成了一定的影响。我当时就看完了...
FDA 2025医疗器械提交电子副本(eCopy)计划行业与 FDA 工作人员指南(eCopy Program for Medical Device Submissions Guidance for Industry and Food and Drug Administration Staff)-附下载
2025 年 12月 3日,美国食品药品监督管理局(FDA)正式发布了更新后的《医疗器械提交电子副本(eCopy)计划行业与 FDA 工作人员指南》。该指南取代了 2020 年 4 月 27 日的旧版内容,进一步明确...
202512-加拿大卫生部HC-Guidance on nitrosamineimpurities in medications药物中亚硝胺杂质的风险管控与合规要求-附下载
2025 年 8 月 1 日,加拿大健康部(Health Canada)正式实施了更新后的《药物中亚硝胺杂质指南》,对人用药品、生物制品和放射性药品中的亚硝胺杂质风险评估、检测验证及市场授权变更等提出了全...
资源分享-202505细胞治疗产品IND申报药学技术一般考虑PPT-陈超等
文档结构概述 文档分为四个主要部分,逻辑清晰,从基础概念到实际应用,再到案例和总结: 概述(页1-9) 这部分介绍了细胞治疗产品的基本概念、分类和发展现状。 定义:细胞治疗产品是...
重磅资料分享-药品生产场地变更汇总国家局及各省局
允咨医药培训中心对国家局及各省局药品生产场地变更相关问答与实施细则进行汇总,内容涵盖变更分类(重大、中等、微小变更)、不同场景(省内 / 省外委托生产、企业内部车间变更、长期未生产恢...
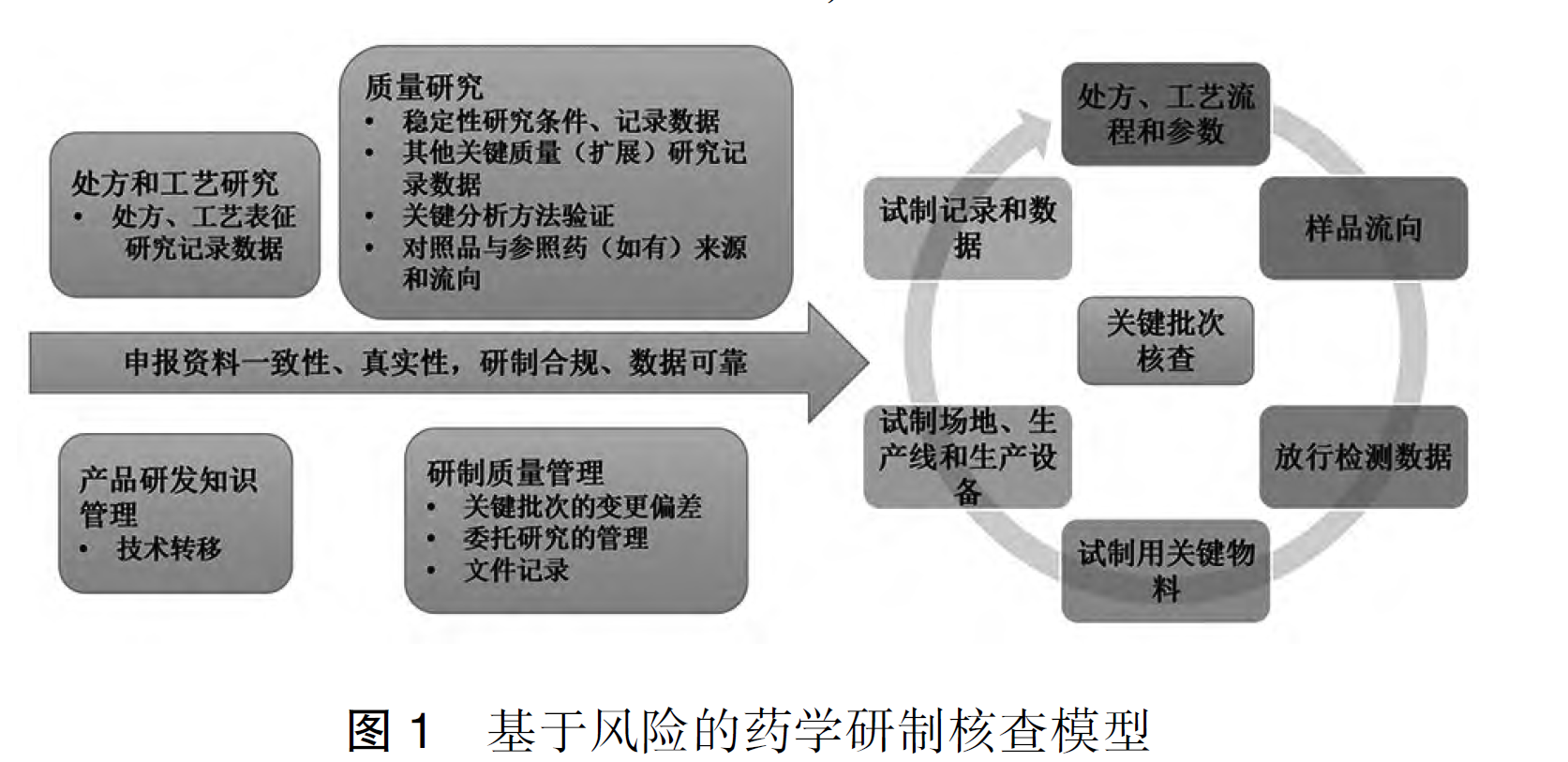
重磅文献分享-生物制品药学研制核查要点和常见问题分析(2025 CFDI 张平)-附下载
摘要 生物制品的生产和质量控制过程中,存在诸多可变性和特殊性。在新的药品注册监管法规体系下,研制现场核查是促进生物制品研发相关数据真实可追溯,推动生物制品研发行业规范和高质量发展...
文献分享-MAH制度下集团型企业一体化质量管理模式的实践与探索(附下载地址)
在药品上市许可持有人(MAH)制度全面实施的当下,中国制药行业正迎来一场深刻的管理变革。近日,由赛诺菲阮克萍、陈洁、张羽嘉、李茜等专家联合撰写的重磅论文——《MAH制度下集团型企业一体化...
202512-MHRA-Good Clinical practice for clinical trails(2025版 MHRA GCP 指南)-附下载
作为临床试验领域的核心监管标准,良好临床规范(GCP)是保障受试者权益、确保试验数据真实可靠的基石。英国药品和健康产品管理局(MHRA)于 2025 年 12 月更新的《临床试验良好临床规范指南》...
省局发布《江苏省药品上市后生产场地变更优先受理审评实施细则(试行)》
2024年11月06日,江苏省局发布《江苏省药品上市后生产场地变更优先受理审评实施细则(试行)》(发布之日起实施)。该文件曾在2024年08月05日发布征求意见稿。 文件的目的是加速药品上市后生...
202511- PDA-CCS作为生产力之路:洁净室再认证CCS as A Path to Productivity:Cleanroom Requalification-附下载
在制药行业,洁净室是保障无菌药品质量与安全的核心设施。根据 PDA(注射药物协会)定义,洁净室是通过设计、维护和控制,防止药品受到颗粒和微生物污染的专用空间,其空气洁净度需达到并持续满...

















kidzhangy6月前0
感谢分享,楼主好人一生平安Terrific7月前0
感谢!特别有用,资源分享的很及时!北岛2年前0
相当于货架期多久?Mark4年前2
Thanks for your blog, nice to read. Do not stop.一位WordPress评论者5年前0
嗨,这是一条评论。 要开始审核、编辑及删除评论,请访问仪表盘的“评论”页面。 评论者头像来自Gravatar。