排序
FDA 7346.832M 全解读:2026 生物制品 GMP & 数据完整性检查-附双语版下载
2026 年 4 月,FDA 正式发布7346.832M 合规计划,并于5 月 14 日全面实施。这份长达 83 页的指南,是 CDER 针对蛋白类生物制品生产商的上市前许可检查 (PLI)与批准前检查 (PAI) 的核心依据,直...
PDA-TR56-阶段适宜性质量体系与药品生产质量管理规范在生物药原液研发中的应用2026修订版-附下载
近日,Parenteral Drug Association(PDA)正式推出《PDA 技术报告第 56 号(修订版):阶段适宜性质量体系与药品生产质量管理规范在生物药原液研发中的应用》(以下简称 TR56 2026 修订版)。...
20260320-EMA-Chemistry of active substances (chemistry of new active substances)活性物质的化学指南-附下载
欧盟药品管理局(EMA)于2026年2月16日正式采纳并发布了修订版《活性物质的化学指南》(Guideline on the chemistry of active substances,EMA/CHMP/QWP/49484/2026),该指南将于2026年9月1日...
资源分享-台湾-运用奈米技术承载 siRNA 药品之指导原则20260318
中国台湾地区财团法人医药品查验中心于 2026 年 3 月 18 日发布的第一版《运用奈米技术承载 siRNA 药品之指导原则》,是当地首部针对该领域的专项监管指引,参考日本 MHLW 相关规范制定,适用于...
资源分享-APIC-亚硝胺杂质潜在风险评估报告模板
这份文件是 APIC 推出的亚硝胺杂质潜在风险评估报告模板,专为活性药物成分(API)制造商设计,核心用于系统性评估 API 生产及储存过程中亚硝胺杂质的潜在存在风险,助力企业合规满足国际监管要...
资源分享-RDPAC-国内外药品技术指导原则体系对比研究(药学部分)
该文件是 2022 年 11 月由国家药品监督管理局药品审评中心、中国药品监督管理研究会等多机构联合发布的研究报告,聚焦国内外药品技术指导原则体系的药学部分,旨在推进我国相关体系与国际接轨、...
资源分享-2025年识林法规指南导航全球药监
这份文件是识林发布的 2025 年全球药监法规指南报告,聚焦中国、美国、欧盟等六大官方机构发布的 811 份高价值监管文件,围绕监管政策、非临床与临床研究、药学研究、注册与变更等 7 个药品全生...
2025-EMA-HUMAN MEDICINES IN 2025 (2025人用药物年度报告)-附下载
2025 年,欧洲药品管理局(EMA)交出了一份亮眼的药品监管与创新成绩单。从 104 个新药积极授权意见到罕见病治疗的突破性进展,从生物类似药的爆发式增长到全球公共卫生的跨区域协作,这一年的...
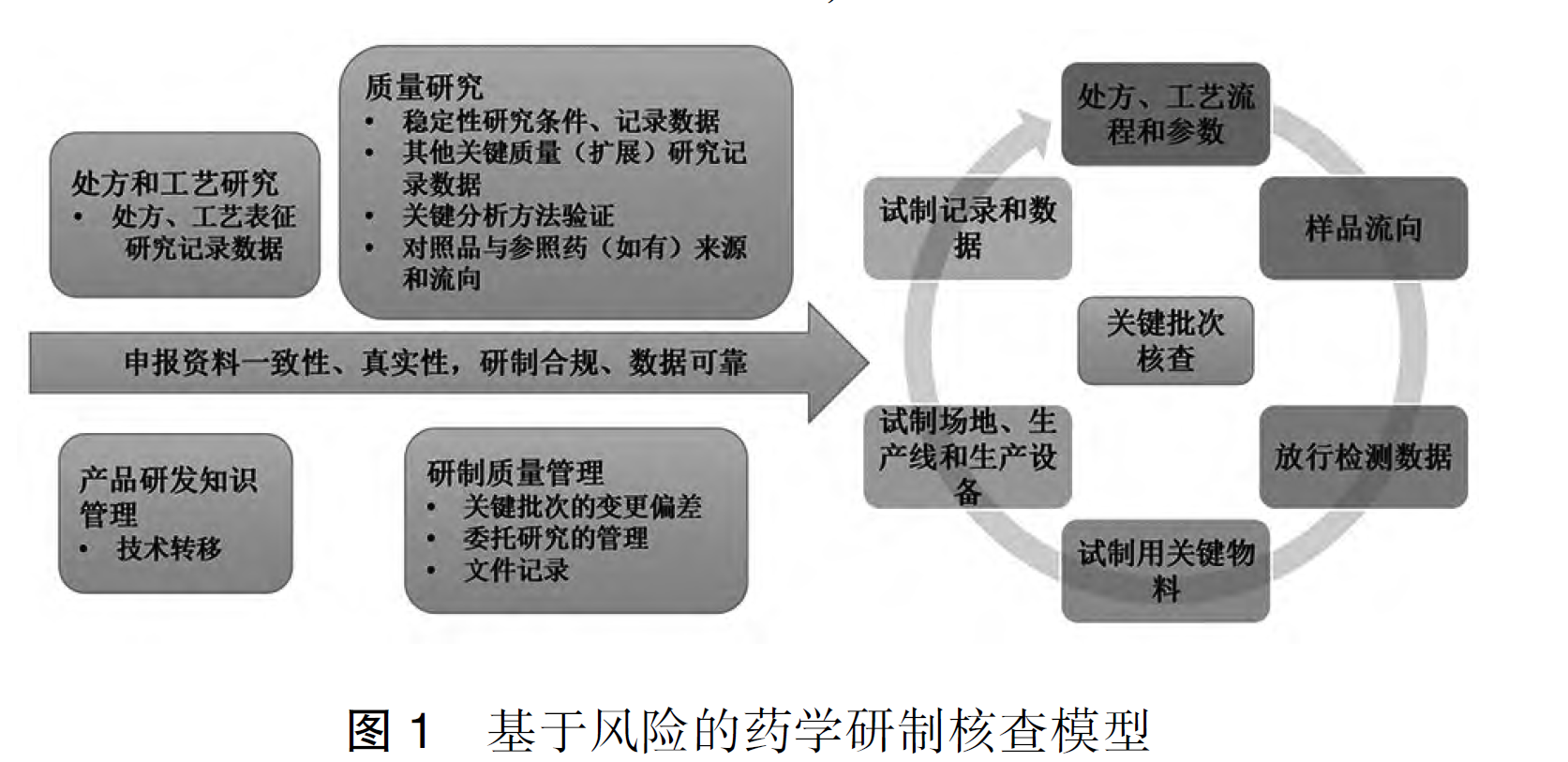
重磅文献分享-生物制品药学研制核查要点和常见问题分析(2025 CFDI 张平)-附下载
摘要 生物制品的生产和质量控制过程中,存在诸多可变性和特殊性。在新的药品注册监管法规体系下,研制现场核查是促进生物制品研发相关数据真实可追溯,推动生物制品研发行业规范和高质量发展...
202406-官方培训-药品共线生产与清洁验证专题培训班培训讲义(宁波)
该文件是国家药品监督管理局高级研修学院 2024 年 6 月宁波专题培训班的培训讲义,核心围绕《药品共线生产质量风险管理指南》展开,系统涵盖指南起草背景、核心原则(法律法规优先、持有人主责...















kidzhangy6月前0
感谢分享,楼主好人一生平安Terrific7月前0
感谢!特别有用,资源分享的很及时!北岛2年前0
相当于货架期多久?Mark4年前2
Thanks for your blog, nice to read. Do not stop.一位WordPress评论者5年前0
嗨,这是一条评论。 要开始审核、编辑及删除评论,请访问仪表盘的“评论”页面。 评论者头像来自Gravatar。