排序
ECA-审计追踪审查通用SOP征求意见稿2025-附下载
本文件基于风险评估,提供了一个清晰的框架,帮助制药企业确保患者安全和产品质量。下面,我将解读这份文件的要点,并结合实际应用分享我的见解。 文件概述 指导GMP计算机化系统的审计轨...
资源分享-临床前动物安评的管理(法规要求和注意事项)
文件从法规、实操、合作管理三个维度,聊聊临床前动物安评的那些关键要点。 链接:https://pan.quark.cn/s/7661c7f29ec8
202512FDA指南-Promotional Labeling and Advertising Considerations for Prescription Biological Reference Products, Biosimilar Products, and Interchangeable Biosimilar Products Questions and Answers 生物类似药促销宣传的合规指南问答-附下载
2025 年 12 月,美国食品药品监督管理局(FDA)发布了《处方药生物参考产品、生物类似药和可互换生物类似药的促销标签和广告考量问答指南》,为制药企业的合规宣传提供了明确指引。在生物类似药...
资源分享-202512-欧洲药典凡例(中英文对照 EP11.0)
该文件为《欧洲药典》11.0 版凡例(含 12.1 版相关修订说明)的中英文对照文本,核心围绕药典的适用规则、技术规范及相关要求展开。12.1 版因药典转为纯在线格式,修订了出版周期术语(“版本或...
书籍分享-图解GMP检查要点-张金贵主编(202509)
《图解 GMP 检查要点》由张金贵编著、中国医药科技出版社 2025 年 9 月出版,以《药品生产质量管理规范 (2010 年修订)》的 13 章 309 个条款为核心,创新采用 “思维导图 + 要点剖析” 的呈现形...
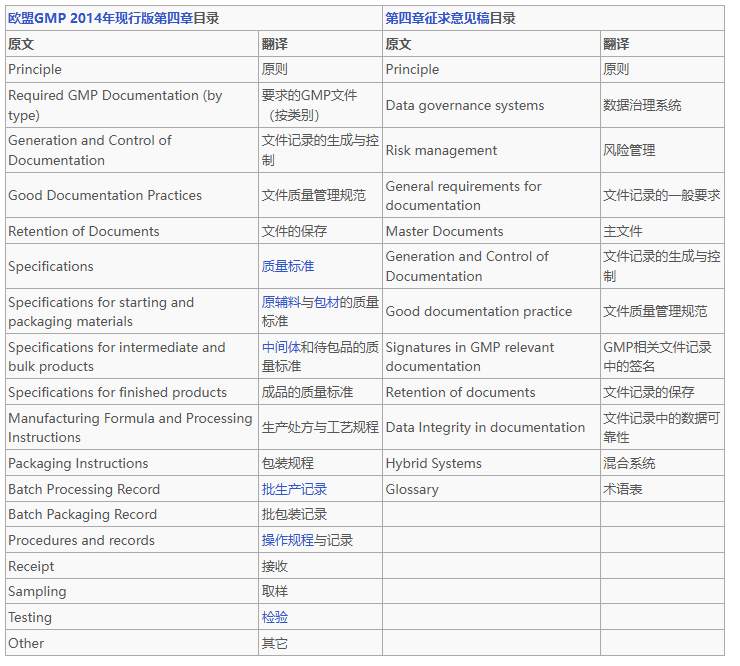
EU GMP发布第四章Documentation文件管理征求意见稿-文末附双语版下载地址
随着制药行业的不断发展,欧盟良好生产规范(EU GMP)也在持续更新,以适应技术进步和监管需求的变化。EU GMP 第四章“文件管理”是质量管理体系的核心组成部分,其修订对制药企业的合规性和运...
资源分享-药物研发基本原理 中文翻译版 第2版-本杰明-科学出版社
本书从药物发现与开发的历程开始, 为读者呈现了药物发现的经典靶点、体外筛选系统、 体内筛选模型、药物化学和药代动力学研究等新药研究的基本原理和方法, 同时介绍了药物临床前和临床研究过...
ASTM E2656-25 标准实践——制药用水中总有机碳(TOC)属性的实时释放测试指南(Standard Practice for Real-time Release Testing of Pharmaceutical Water for the Total Organic Carbon Attribute)-附下载地址
在药品和生物制药制造中,水是使用最广泛的成分或原料。其纯度,特别是总有机碳(TOC)含量,直接关系到最终产品的质量。传统上,我们依赖于实验室取样和分析的模式进行水质放行,这种模式耗时...
202511- PDA-CCS作为生产力之路:洁净室再认证CCS as A Path to Productivity:Cleanroom Requalification-附下载
在制药行业,洁净室是保障无菌药品质量与安全的核心设施。根据 PDA(注射药物协会)定义,洁净室是通过设计、维护和控制,防止药品受到颗粒和微生物污染的专用空间,其空气洁净度需达到并持续满...
ISPE-Building a Quality Culture via Software Quality Engineering软件质量工程(SQE)塑造制药行业质量文化-附下载
在数字化浪潮席卷全球的今天,制药行业正经历着从 “自动化” 到 “智能化” 的深度变革,Pharma 4.0 不再是遥远的概念,而是关乎企业竞争力的核心命题。2025 年 10 月,在夏洛特举办的 ISPE(...




















kidzhangy5月前0
感谢分享,楼主好人一生平安Terrific6月前0
感谢!特别有用,资源分享的很及时!北岛2年前0
相当于货架期多久?Mark4年前2
Thanks for your blog, nice to read. Do not stop.一位WordPress评论者5年前0
嗨,这是一条评论。 要开始审核、编辑及删除评论,请访问仪表盘的“评论”页面。 评论者头像来自Gravatar。