排序
FDA指导原则合集(FDA Guidance Documents)-持续更新
本文持续更新FDA的指导原则并打包,方便离线检索查阅,内容覆盖从FDA发布的从1975至今的所有指导原则,截至2025年7月22日,FDA共发布2275个指南文件。
药品管理法实施条例2026第四次修订-新旧对比,CMC相关重点变化内容解读
2026年1月16日中华人民共和国国务院令第828号第四次修订《药品管理法实施条例》,新版条例将于2026年5月15日起施行 新旧版本对比 中华人民共和国药品管理法实施条例旧中华人民共和国药品...
资源分享-202512-EMA-Guideline on stability testing for applications for variations to a marketing authorisation(EMA 稳定性试验变更指南)
2025 年 12 月,欧洲药品管理局(EMA)发布了修订后的《上市许可变更申请稳定性试验指南》(EMA/CHMP/QWP/441071/2011-Rev.3),该指南将于 2026 年 1 月 15 日正式生效,全面替代 2011 年版 Re...
资源分享-大湾区202509药品注册生产现场核查与符合性检查衔接工作程序介绍
对于药企而言,药品注册生产现场核查与上市前 GMP 符合性检查是药品上市前的关键环节。国家层面出台的衔接工作程序,不仅明确了核查检查的核心规则,更直接影响企业的注册效率与合规成本。今天...
202512-黑龙江药监-关于《关于修订〈黑龙江省药品上市后场地变更实施办法(试行)〉及部分条款有关事宜的通知》的政策解读
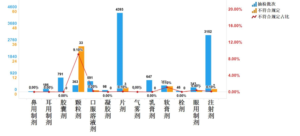
各药品上市许可持有人、药品生产企业,机关各处室、各直属单位: 2022年10月,我局出台《黑龙江省药品监督管理局药品上市后场地变更实施办法(试行)》(简称《办法》,通过优化许可检查,促...
20251203-CDE重磅发布!《化学仿制药药学研究重大缺陷(试行)》征求意见稿解析-附下载
2025年12月3日,CDE发布通知,公开征求《化学仿制药药学研究重大缺陷(试行)(征求意见稿)》等文件的意见 。这份文件不仅仅是一个技术清单,更是一次审评逻辑的重大调整。核心内容在于:对于...
转载-2025年CDE官方问答全梳理(截至20260109)
2025年,国家药品监督管理局药品审评中心(CDE)持续围绕药品注册申报中的关键环节、高频疑问与共性难题,发布了一系列具有指导意义的共性问题解答。为帮助业界更清晰把握政策导向、提升申报效...
资源分享-202512-CDE-放射性新药要学审评中常见问题和考虑-周浩晖
该文件是药审中心化药药学一部 2025 年 12 月发布的关于放射性新药药学审评的专业指引,明确了放射性药品(用于临床诊断或治疗的放射性核素制剂或其标记药物)的发展现状(传统企业与新入局企业...
资源分享-2025年识林法规指南导航全球药监
这份文件是识林发布的 2025 年全球药监法规指南报告,聚焦中国、美国、欧盟等六大官方机构发布的 811 份高价值监管文件,围绕监管政策、非临床与临床研究、药学研究、注册与变更等 7 个药品全生...
资源分享-202512-CDE-放射性化学仿制药药学审评的关注点和考虑-何艳
该培训阐述了该类药物具有放射性、定制生产或即时标记、按放射性活度给药等特殊特点,梳理了《放射性化学仿制药药学研究技术指导原则》等相关技术要求文件的制定历程及已发布、待发布情况,明确...



















kidzhangy6月前0
感谢分享,楼主好人一生平安Terrific7月前0
感谢!特别有用,资源分享的很及时!北岛2年前0
相当于货架期多久?Mark4年前2
Thanks for your blog, nice to read. Do not stop.一位WordPress评论者5年前0
嗨,这是一条评论。 要开始审核、编辑及删除评论,请访问仪表盘的“评论”页面。 评论者头像来自Gravatar。