排序
202512-MHRA-Good Clinical practice for clinical trails(2025版 MHRA GCP 指南)-附下载
作为临床试验领域的核心监管标准,良好临床规范(GCP)是保障受试者权益、确保试验数据真实可靠的基石。英国药品和健康产品管理局(MHRA)于 2025 年 12 月更新的《临床试验良好临床规范指南》...
书籍推荐-《The ASQ Certified Quality Engineer Handbook》(ASQ 认证质量工程师手册)第五版
本书是《The ASQ Certified Quality Engineer Handbook》(ASQ 认证质量工程师手册)的第五版,由 Scott A. Laman 编辑,出版于 2022 年,由 ASQExcellence 发行。全书总页数超过 576 页(从目...
资源分享-202512-药品注册审评缺陷研究-by zhulikou431(丁恩峰老师)
这份由丁香园 zhulikou431 (丁老师)编写的《药品注册审评缺陷研究》(R139修订本)是一部深度汇总了2010年至2025年跨度的药品注册案例集,旨在通过分析CDE(药审中心)在审评审批中提出的缺陷...
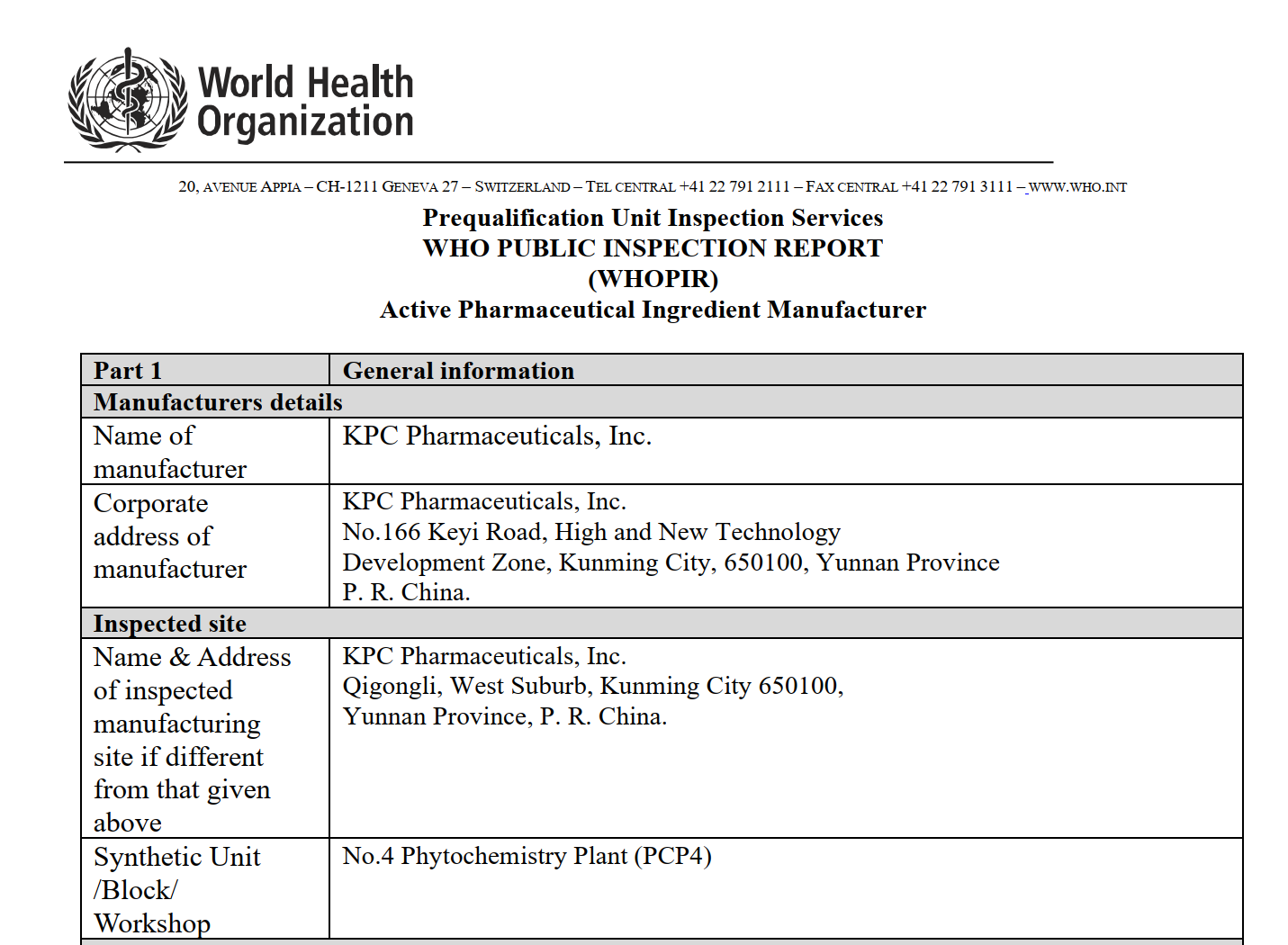
从昆明制药WHO检查报告看API企业的国际化合规道路-附下载
近期,世界卫生组织(WHO)发布了针对昆明制药集团股份有限公司(KPC Pharmaceuticals, Inc.)的公开检查报告(WHOPIR)。此次审计于2025年6月9日至13日进行,旨在对其生产的原料药(API)蒿甲...
20251206-CDE第十二期药审云答疑问题汇总
问题1:2.6生产工艺的开发部分,是否应该将小试阶段做过的所有(均体现),还是说仅汇总关键工艺参数相关的即可? 解答1:工艺开发部分对于原料药申报资料很重要。对于仿制药来说,首先应基...
资源分享-20251205-江苏药监-江苏药品委托生产现场检查常见缺陷分析(南京分中心)
江苏省药品监督管理局审评核查南京分中心于 2025 年 12 月 5 日举办的药品委托生产现场检查常见缺陷分析培训,系统梳理了药品委托生产过程中在机构与人员、共线生产管理、委托生产管理等多个关...
2019-奥星-Compilation of Global Data Integrity Regulations & Guidance全球数据可靠性法规指南汇编(第 6 版)-附下载
数据可靠性指南汇编,方便大家学习,文件截至2019年10月,部分文件不是最新 链接:https://pan.quark.cn/s/9e9d376ecebb
20251211-上海药监-上海市药品主动召回实施指南(征求意见稿)》发布-附下载
背景 药品召回是保障公众用药安全的关键环节。根据国家《药品召回管理办法》和相关规定,药品上市许可持有人(简称“持有人”)必须主动监测风险,并在发现质量问题或安全隐患时及时召回。这...
资源分享-202512-CDE-放射性化学药品非临床评价策略和关注点-赵春阳
这份培训内容围绕放射性化学药品(含诊断与治疗类,以 RDC 为主,涉及多种核素、配体 / 载体及新靶点)的非临床评价展开,涵盖我国放药研发与政策背景、相关指导原则框架,明确非临床研究需遵循...
202510奥星-全球法规趋统背景下的产品共线生产与清洁验证-附下载
该 文件围绕全球法规趋同背景下的药品共线生产与清洁验证展开,系统介绍了共线生产的概念及国内外相关法规要求,聚焦产品全生命周期(研发、技术转移、生产、上市后)的清洁验证管理,详解了清...



















kidzhangy5月前0
感谢分享,楼主好人一生平安Terrific6月前0
感谢!特别有用,资源分享的很及时!北岛2年前0
相当于货架期多久?Mark4年前2
Thanks for your blog, nice to read. Do not stop.一位WordPress评论者5年前0
嗨,这是一条评论。 要开始审核、编辑及删除评论,请访问仪表盘的“评论”页面。 评论者头像来自Gravatar。