排序
资源分享-CFDI20251015生物制品厂房设施设计与风险控制考虑-厂房设施设计中的无菌保障实践-杨冕
在生物制药行业,厂房设施不仅是生产载体,更是产品质量与安全的 “第一道防线”。尤其是抗体药物、ADC 等生物大分子药物,其生产工艺的复杂性、敏感性对厂房设计提出了极高要求 —— 既要满足 ...
好书推荐-中国药品检验系列丛书-分析方法开发验证转移和确认-王思寰-中国医药科技出版社202404
《分析方法开发、验证、转移和确认》由王思寰等编著,2024 年 4 月由中国医药科技出版社出版,聚焦药品分析方法全生命周期管理,为相关从业者提供系统指导。全书共十二章,以法规指南为依托,融...
资源分享-202512-药品注册审评缺陷研究-by zhulikou431(丁恩峰老师)
这份由丁香园 zhulikou431 (丁老师)编写的《药品注册审评缺陷研究》(R139修订本)是一部深度汇总了2010年至2025年跨度的药品注册案例集,旨在通过分析CDE(药审中心)在审评审批中提出的缺陷...
资源分享-2025年医药行业年终总结-政策篇(易联招采网)
这份 文件是《2025 年医药行业年终总结政策篇》(236张幻灯片),主要内容是对 2025 年医药行业政策环境的全面总结和分析。 PPT 涵盖了医药行业的多个重要政策领域:从医药卫生体制改革、药...
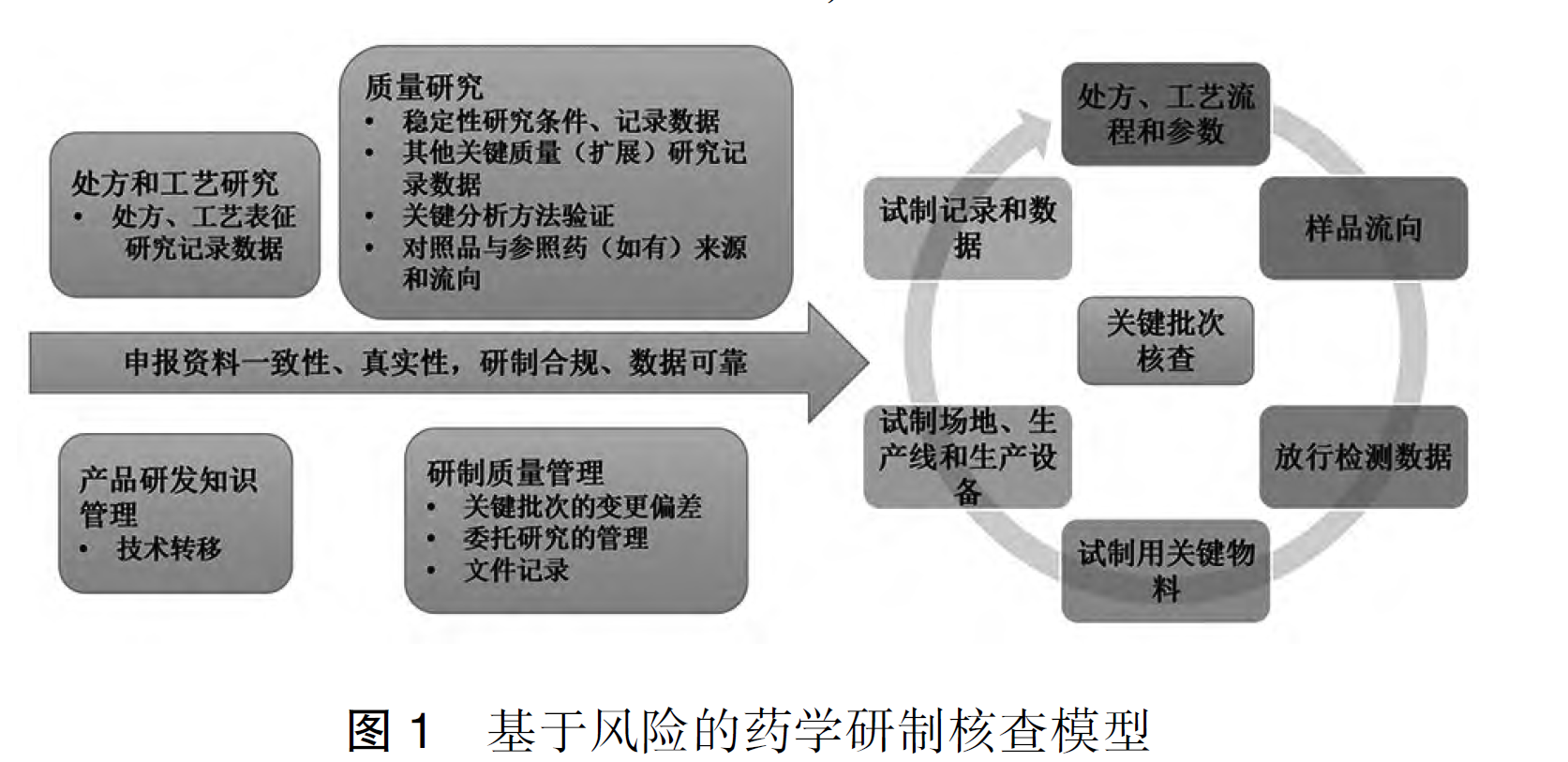
重磅文献分享-生物制品药学研制核查要点和常见问题分析(2025 CFDI 张平)-附下载
摘要 生物制品的生产和质量控制过程中,存在诸多可变性和特殊性。在新的药品注册监管法规体系下,研制现场核查是促进生物制品研发相关数据真实可追溯,推动生物制品研发行业规范和高质量发展...
欧盟GMP发布附录11征求意见稿-文末附各版本及双语版本下载地址
随着信息技术在制药行业的深入应用,计算机化系统的合规管理愈发关键。欧盟GMP附录11是指导这一领域的核心文件,其2011年版已实施多年,而2025年征求意见稿则顺应技术进步和监管需求进行了更新...
资源分享:PDA技术报告TR26 液体除菌过滤Sterilizing Filtration of Liquids(2025 Revised)
资源概述今天为大家分享的是制药行业权威指南 ——PDA TR-26 (Revised 2025): Sterilizing Filtration of Liquids(液体除菌过滤技术报告)。这份由注射药物协会(Parenteral Drug Association,...
资源分享-细胞库和毒种库制备的管理
细胞库与毒种库是疫苗、抗体药物等产品生产的 “源头根基”。其质量直接决定了最终产品的安全性、有效性与稳定性,而科学规范的制备管理则是守住这一源头安全的核心防线。本文件从法规合规、风...
20251209-黑龙江药监问答汇总(药品审评-疫苗-经营-生产检查相关)
药品审评问答 1.《已上市化学药品药学变更研究技术指导原则(试行)》规定,某些中等变更需提供1~3批检验报告,请问具体应该提供几批? 答:指导原则中检验报告批次的设定范围(1~3批)...
资源分享-药典凡例-印度药典(2022)
《印度药典 2022 年版(IP 2022)凡例》为药典标准、试验、测定及正文表述等提供基本指导原则,明确了法定药品(含法定物质、制剂)的定义与适用范围(含人用和兽药,除非明确限定),规定药品...



















kidzhangy5月前0
感谢分享,楼主好人一生平安Terrific6月前0
感谢!特别有用,资源分享的很及时!北岛2年前0
相当于货架期多久?Mark4年前2
Thanks for your blog, nice to read. Do not stop.一位WordPress评论者5年前0
嗨,这是一条评论。 要开始审核、编辑及删除评论,请访问仪表盘的“评论”页面。 评论者头像来自Gravatar。