排序
202509-EMA-Guidelines on the details of the various categories of variation欧盟药品上市许可变更新指南(2026生效)-附下载
2026 年 1 月 15 日,欧盟《药品上市许可变更分类及流程指南》(C/2025/5045)将正式生效,替代沿用 13 年的 2013 版指南。这份经 2024 年修订的新规,通过简化流程、优化分类、强化工作共享机...
资源分享-某制药企业基于主数据数字化转型项目蓝图规划汇报方案
这份文件是某制药企业 2021 年数字化转型项目蓝图规划汇报,围绕业务流程框架、应用支撑框架等八大议程展开,聚焦寻源到付款、计划到产出、订单到收款、全面质量管理、财务管理转型等关键业务领...
2025年第六期“药审云课堂”-课件和培训视频分享
6月6日,CDE进行了2025年度第六期药审云培训,本期以“药品注册申报常见问题”为主题,系统展示药品注册申报流程及多层级多渠道沟通交流机制,让公众更好地了解药品审评工作,同时帮助申请人科...
资源分享-山东药监-药品GMP检查手册(上,下)
本书是专为药品GMP检查员、监管人员和药企从业者设计的便携式工具书。它于2021年2月发布,旨在配合新药品管理法的实施,推动药品生产质量管理水平的提升。 上册(法规篇):基础法律法规...
资源分享IND注册申报要求及注意事项
在创新药研发的漫长征程中,IND(Investigational New Drug,新药临床研究审批)申报是连接临床前研究与临床试验的关键桥梁。它不仅是对药物安全性和临床方案合理性的官方检验,更是药企合规研...
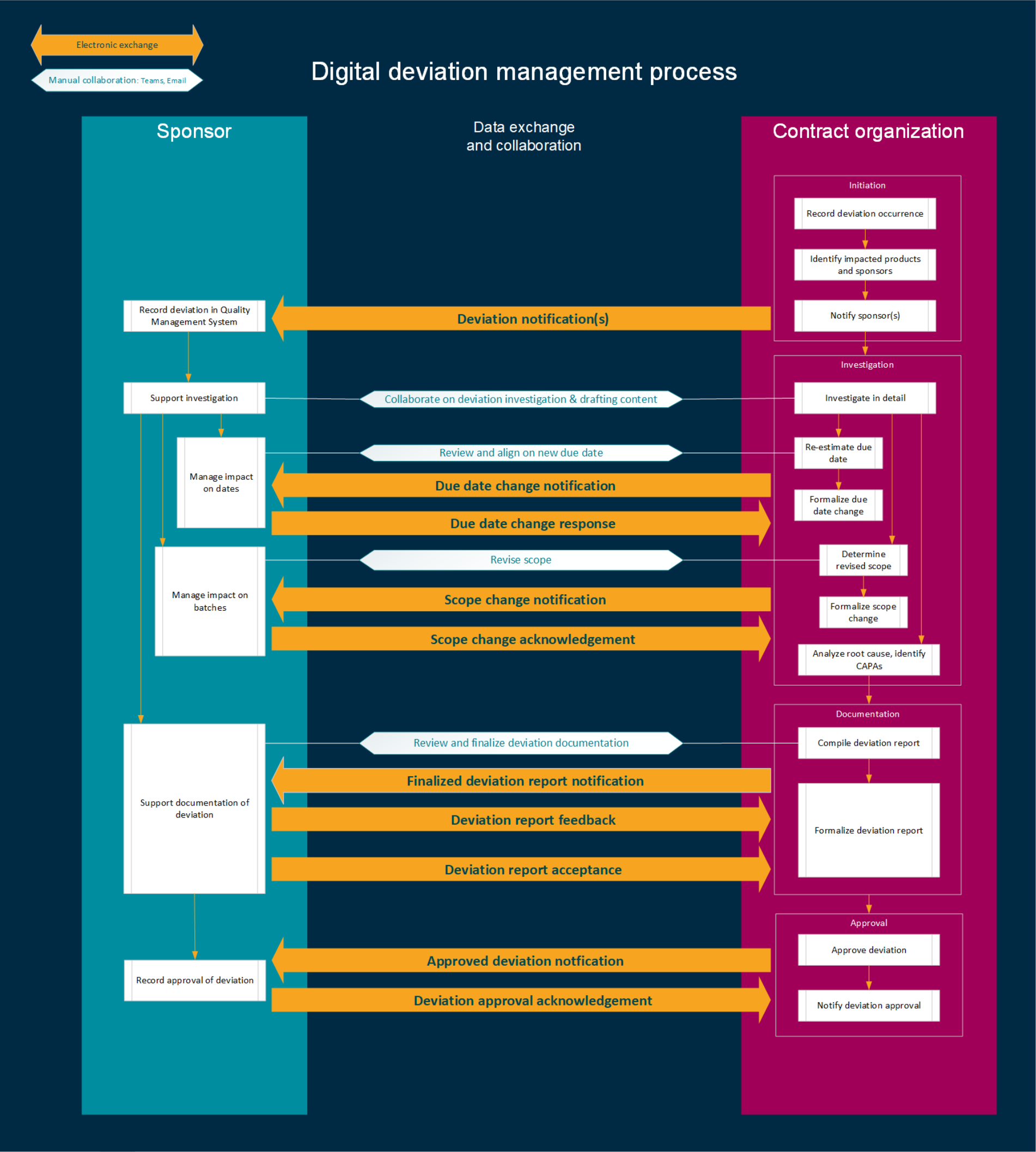
委托生产的数字化偏差管理协同(Digital deviations: Improving sponsor— CMO collaboration-附biophorum双语原文)
摘要 在生物制药行业内管理偏差是确保产品质量、法规合规性以及最终患者安全的关键流程。如今,委托方与合同制造组织(CMOs)之间的偏差管理过程高度依赖人工操作,复杂且分散,导致效率低...
资源分享-202512-日本药典凡例中英双语(JP18)
该文件为日本药典第十八版(JP XVIII)凡例,明确了药典官方名称及缩写,界定了 JP 药品(含药材及相关制品、复方制剂等)的定义与法定名称规则,规定药品需依据相关各论、通用注意事项等进行检...
202512-CDE化学仿制药共性问题汇总(202312-202512)
学习/整理CDE公开的“化学仿制药共性”问题,从2023年12月至2025年12月,共计38条。 1.根据ICH Q3D指导原则及2025年版《中国药典》,如何进行化学原料药中元素杂质的评估和控制? A:一、...
21 CFR Part 312 Investigational New Drug Application (IND)-新药临床试验申请 中英文双语对照
《21 CFR Part 312》是美国食品药品监督管理局(FDA)制定的关于新药临床试验申请 (IND)的管理法规,规定了药物在正式上市前开展临床研究的全过程监管要求。该法规最初于 1987 年发布,...
EMA PMS FAQ:欧洲药品管理局的产品管理服务常见问题解答202511(Product Management Service (PMS) – Frequently Asked Questions (FAQs))-附下载地址
《Product Management Service (PMS) – Frequently Asked Questions (FAQs)》,发布于2025年11月21日。它汇集了PMS相关活动中通过Slido.com收集的常见问题,并按主题分类解答。作为医药监管领...




















kidzhangy5月前0
感谢分享,楼主好人一生平安Terrific6月前0
感谢!特别有用,资源分享的很及时!北岛2年前0
相当于货架期多久?Mark4年前2
Thanks for your blog, nice to read. Do not stop.一位WordPress评论者5年前0
嗨,这是一条评论。 要开始审核、编辑及删除评论,请访问仪表盘的“评论”页面。 评论者头像来自Gravatar。