排序
202511-PDA-从极端污染控制失败中吸取教训Contamination Control Failures-What we learn from worst case scenarios-附下载
在生物制药行业,无菌生产是不可逾越的红线,而污染控制则是守护这条红线的核心防线。然而,即使是流程规范的药企,也可能因看似微小的疏忽陷入污染危机。近日,Parenteral Drug Association(P...
20211118-CDE-eCTD专题培训课件
2021年11月18日国家药品审评中心(CDE)主办的“中国eCTD进展情况概述”专题培训会的完整系列材料,共五份PPT,涵盖了eCTD从政策解读、技术规范、实施指南、申报流程到企业最佳实践的全链条内容...
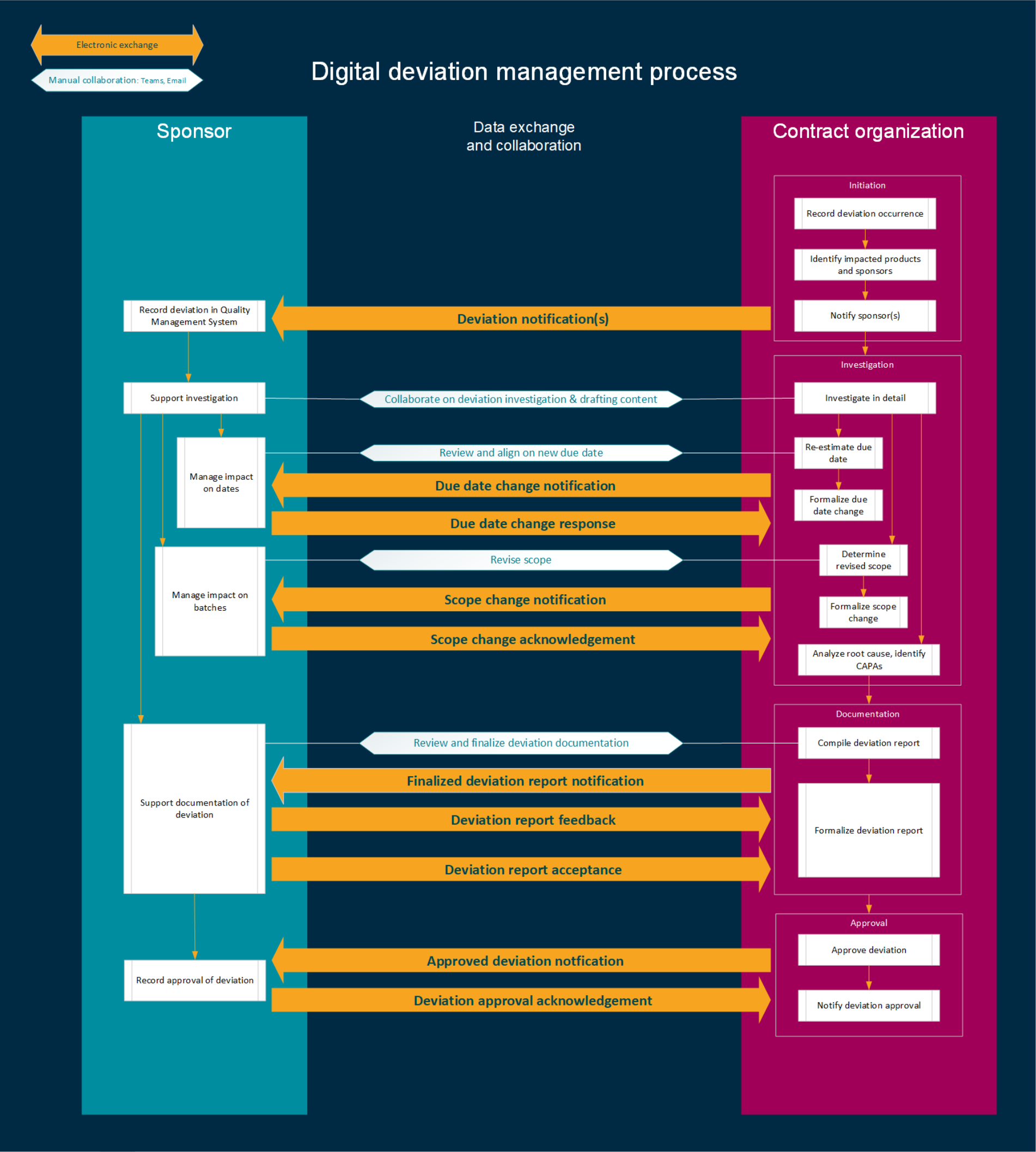
委托生产的数字化偏差管理协同(Digital deviations: Improving sponsor— CMO collaboration-附biophorum双语原文)
摘要 在生物制药行业内管理偏差是确保产品质量、法规合规性以及最终患者安全的关键流程。如今,委托方与合同制造组织(CMOs)之间的偏差管理过程高度依赖人工操作,复杂且分散,导致效率低...
资源分享-大湾区202509工艺验证方法与商业规模工艺验证
链接:https://pan.quark.cn/s/1ed1ef0d8efa 药品作为特殊商品,其质量直接关系到患者生命健康。工艺验证作为药品生产质量管理的核心环节,是确保生产工艺稳定可控、产品质量持续合规的关键...
资源分享-数字化转型制度清单大全(湘江数评老杨)
该文件是湘江数评老杨整理的企业数字化转型相关制度清单大全,涵盖多维度核心制度体系,包括企业数字化转型全生命周期制度(涉及战略与治理、组织与人才、项目全生命周期、技术平台与数据、运营...
202510-ISPE-Novel Technology Applied to Biologics Manufacturing新技术赋能生物制品生产-附下载
2025 年 10 月 26-29 日,2025 ISPE 年会在美国夏洛特市举办并同步开放虚拟参会,复宏汉霖总裁魏东以《Novel Technology Applied to Biologics Manufacturing》为题,分享了生物制造行业趋势、...
好书推荐-中国药品检验系列丛书-分析方法开发验证转移和确认-王思寰-中国医药科技出版社202404
《分析方法开发、验证、转移和确认》由王思寰等编著,2024 年 4 月由中国医药科技出版社出版,聚焦药品分析方法全生命周期管理,为相关从业者提供系统指导。全书共十二章,以法规指南为依托,融...
资源分享-APIC-亚硝胺杂质潜在风险评估报告模板
这份文件是 APIC 推出的亚硝胺杂质潜在风险评估报告模板,专为活性药物成分(API)制造商设计,核心用于系统性评估 API 生产及储存过程中亚硝胺杂质的潜在存在风险,助力企业合规满足国际监管要...
资源分享-2019-中检院-体外诊断试剂检验技术
《体外诊断试剂检验技术》是《中国食品药品检验检测技术系列丛书》之一,由中国食品药品检定研究院组织编写,于 2019 年出版,是药品检验系统第一部系统完整介绍体外诊断试剂检验技术的专业书。...
资源分享0202501-诺和诺德质量体系基础
文件围绕 ICH Q10 药品质量体系展开,先介绍了 ICH 的历史、愿景及相关指南(如 Q8、Q9、Q11 等),明确 ICH Q10 是 2008 年发布的、基于 ISO 质量管理系统且贯穿产品全生命周期(研发、技术转...



















kidzhangy5月前0
感谢分享,楼主好人一生平安Terrific6月前0
感谢!特别有用,资源分享的很及时!北岛2年前0
相当于货架期多久?Mark4年前2
Thanks for your blog, nice to read. Do not stop.一位WordPress评论者5年前0
嗨,这是一条评论。 要开始审核、编辑及删除评论,请访问仪表盘的“评论”页面。 评论者头像来自Gravatar。