排序
转载-2025年CDE官方问答全梳理(截至20260109)
2025年,国家药品监督管理局药品审评中心(CDE)持续围绕药品注册申报中的关键环节、高频疑问与共性难题,发布了一系列具有指导意义的共性问题解答。为帮助业界更清晰把握政策导向、提升申报效...
批判性思维,而非简单分类——深度解读Waters 白皮书《Critical Thinking, Not Categorization》-附下载地址
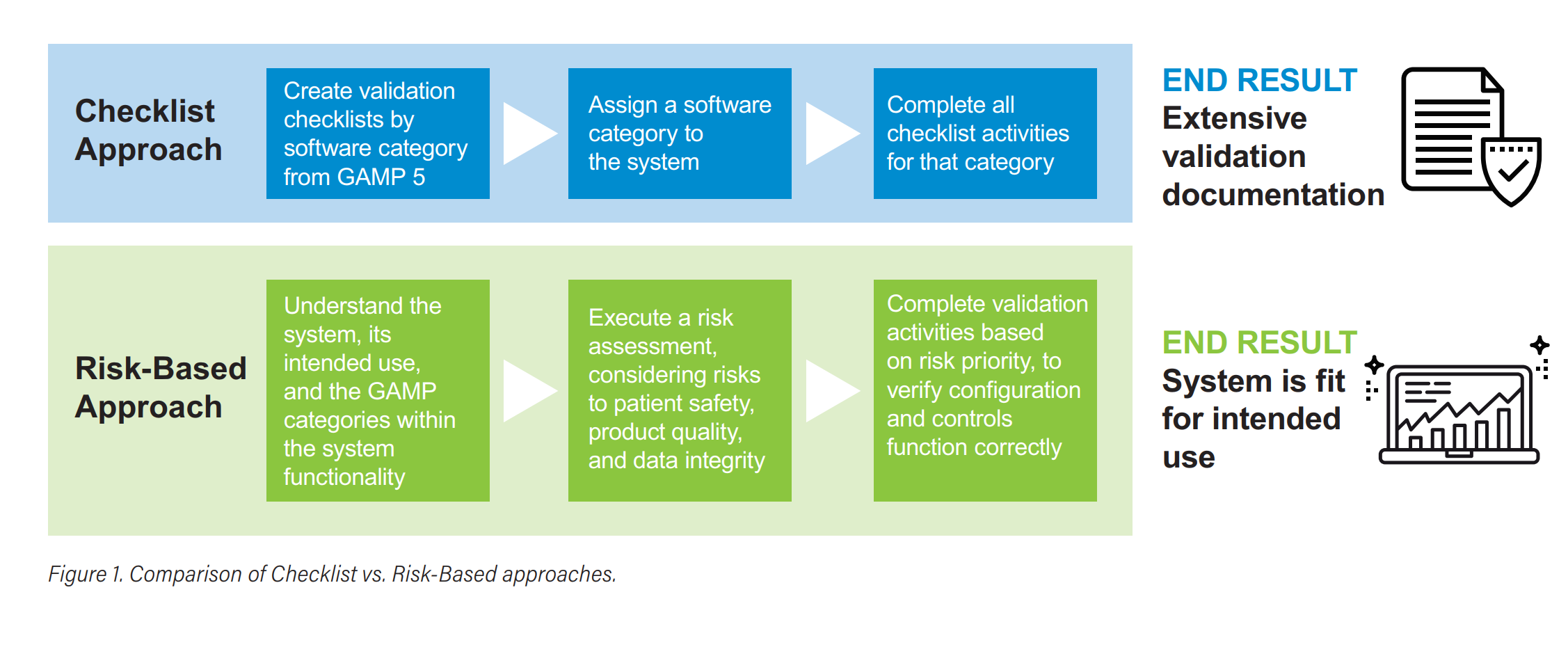
在制药合规圈子里,提到计算机化系统验证(CSV),很多人第一反应就是“这个系统是GAMP几类?我按类别走文档和测试清单就行了”。 但如果你还这么想,真的该好好读读Waters这篇2021年的白皮书了...
资源分享-20251205-江苏药监-江苏药品委托生产现场检查常见缺陷分析(南京分中心)
江苏省药品监督管理局审评核查南京分中心于 2025 年 12 月 5 日举办的药品委托生产现场检查常见缺陷分析培训,系统梳理了药品委托生产过程中在机构与人员、共线生产管理、委托生产管理等多个关...
江苏省局发布药品上市许可持有人药品生产质量安全主体责任清单(2024版)
江苏省局2024年7月份组织的“关于开展企业落实主体责任线上培训”中有提到,省局即将发布的持有人质量安全主体责任正负面清单2024版,替代2023版的清单。 果然08月02日江苏药监发布《关...
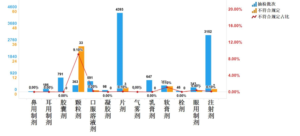
资源分享-生物制品质量研究的管理
药品作为特殊商品,其质量直接关系到患者的生命安全与健康。质量研究作为药品研发、生产、流通全链条的核心支撑,是保障药品安全有效的 “生命线”。从质量标准的建立到异常情况的处置,每一个...
20251209杭州化学放射性药品创新发展宣贯培训答疑整理
问题1:关于放射性药品的规格问题。 老师回复:一般它是一个范围。那么对于注册批次和工艺验证批次,是否要挑战这个边界,生产各六批上限下限的这种要求? 具体考虑如下:对于注册批次和...
海南药监-关于药品变更相关问题的百问百答-附下载
全文下载链接:https://pan.quark.cn/s/edac9bc8417e 第一篇 申报流程 问题 1:药品备案类变更受理形式审查及技术审查流程是什么? 答:1. 申请人提交申请申请人按照《国家药...
20251203-EMA Classification of changes: questions and answers-EMA变更分类新规解析-附下载
欧盟药品管理局(EMA)的变更分类规则直接关系到产品上市后变更的合规推进。2025 年 11 月,EMA 更新了《变更分类问答手册》,针对行政变更、质量变更、(非)临床变更及编辑性变更四大核心场景...
202406-官方培训-药品共线生产与清洁验证专题培训班培训讲义(宁波)
该文件是国家药品监督管理局高级研修学院 2024 年 6 月宁波专题培训班的培训讲义,核心围绕《药品共线生产质量风险管理指南》展开,系统涵盖指南起草背景、核心原则(法律法规优先、持有人主责...
新版《医疗器械生产质量管理规范》正式发布:王昕司长深度宣贯,六大方面全面升级!-附贯宣会PPT
2025年11月17日,国家药监局器械监管司王昕司长亲自进行了《医疗器械生产质量管理规范》(以下简称“新规范”)的线上宣贯。这场宣贯会干货满满、信息量巨大,被业内称为“近年来最重要的一次规...

















kidzhangy5月前0
感谢分享,楼主好人一生平安Terrific6月前0
感谢!特别有用,资源分享的很及时!北岛2年前0
相当于货架期多久?Mark4年前2
Thanks for your blog, nice to read. Do not stop.一位WordPress评论者5年前0
嗨,这是一条评论。 要开始审核、编辑及删除评论,请访问仪表盘的“评论”页面。 评论者头像来自Gravatar。