排序
资源分享-山东药监-药品GMP检查手册(上,下)
本书是专为药品GMP检查员、监管人员和药企从业者设计的便携式工具书。它于2021年2月发布,旨在配合新药品管理法的实施,推动药品生产质量管理水平的提升。 上册(法规篇):基础法律法规...
资源分享IND注册申报要求及注意事项
在创新药研发的漫长征程中,IND(Investigational New Drug,新药临床研究审批)申报是连接临床前研究与临床试验的关键桥梁。它不仅是对药物安全性和临床方案合理性的官方检验,更是药企合规研...
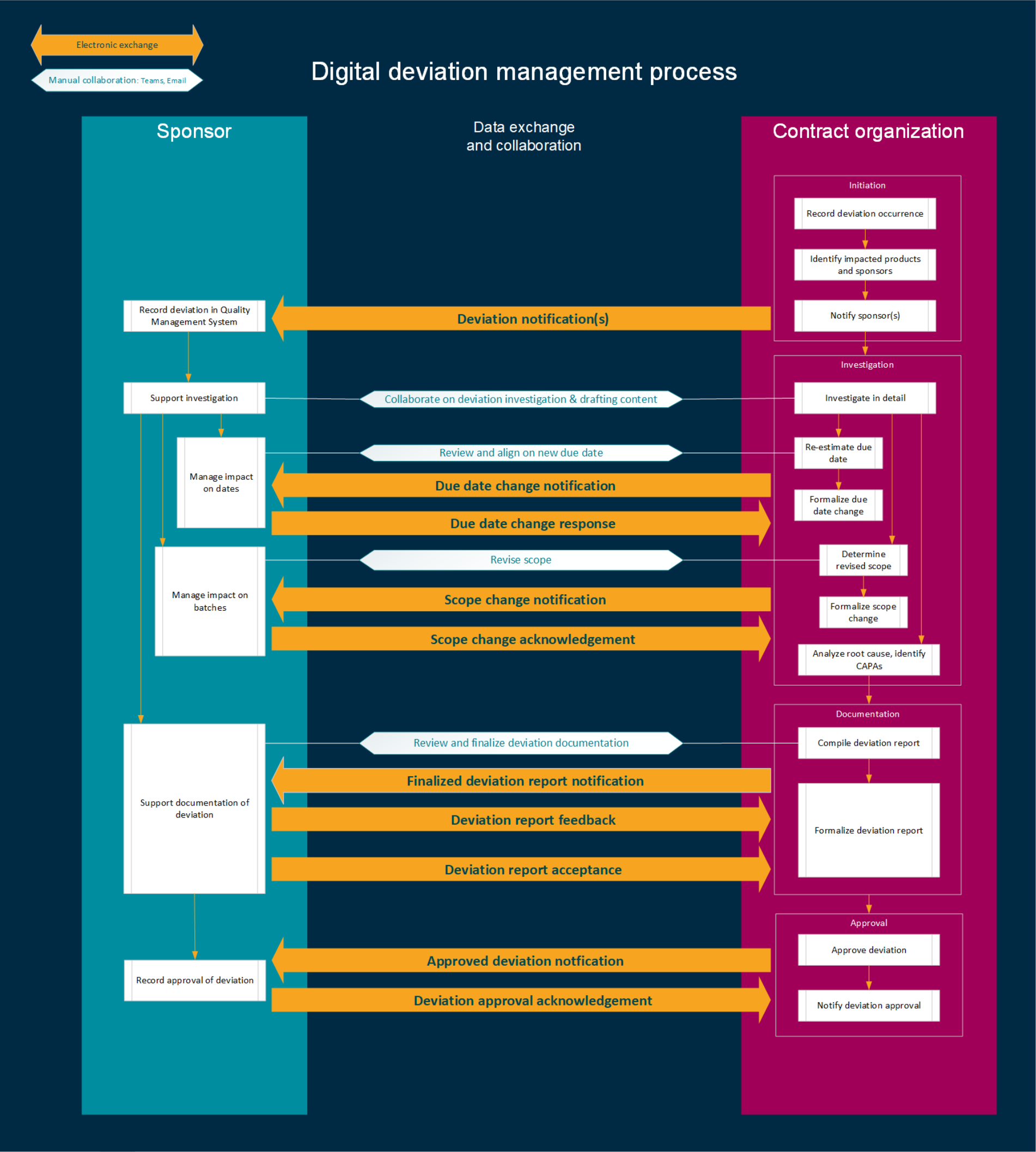
委托生产的数字化偏差管理协同(Digital deviations: Improving sponsor— CMO collaboration-附biophorum双语原文)
摘要 在生物制药行业内管理偏差是确保产品质量、法规合规性以及最终患者安全的关键流程。如今,委托方与合同制造组织(CMOs)之间的偏差管理过程高度依赖人工操作,复杂且分散,导致效率低...
资源分享-202512-日本药典凡例中英双语(JP18)
该文件为日本药典第十八版(JP XVIII)凡例,明确了药典官方名称及缩写,界定了 JP 药品(含药材及相关制品、复方制剂等)的定义与法定名称规则,规定药品需依据相关各论、通用注意事项等进行检...
202512-CDE化学仿制药共性问题汇总(202312-202512)
学习/整理CDE公开的“化学仿制药共性”问题,从2023年12月至2025年12月,共计38条。 1.根据ICH Q3D指导原则及2025年版《中国药典》,如何进行化学原料药中元素杂质的评估和控制? A:一、...
21 CFR Part 312 Investigational New Drug Application (IND)-新药临床试验申请 中英文双语对照
《21 CFR Part 312》是美国食品药品监督管理局(FDA)制定的关于新药临床试验申请 (IND)的管理法规,规定了药物在正式上市前开展临床研究的全过程监管要求。该法规最初于 1987 年发布,...
EMA PMS FAQ:欧洲药品管理局的产品管理服务常见问题解答202511(Product Management Service (PMS) – Frequently Asked Questions (FAQs))-附下载地址
《Product Management Service (PMS) – Frequently Asked Questions (FAQs)》,发布于2025年11月21日。它汇集了PMS相关活动中通过Slido.com收集的常见问题,并按主题分类解答。作为医药监管领...
FDA 2025医疗器械提交电子副本(eCopy)计划行业与 FDA 工作人员指南(eCopy Program for Medical Device Submissions Guidance for Industry and Food and Drug Administration Staff)-附下载
2025 年 12月 3日,美国食品药品监督管理局(FDA)正式发布了更新后的《医疗器械提交电子副本(eCopy)计划行业与 FDA 工作人员指南》。该指南取代了 2020 年 4 月 27 日的旧版内容,进一步明确...
202507-EMA-Review of AI/ML applications in medicines lifecycle (2024)药品生命周期内人工智能和机器学习的应用-附下载
当 AlphaFold 精准预测蛋白质结构加速药物靶点发现,当数字孪生技术缩减临床试验周期,当 AI 算法实时监测上市药物的安全信号 —— 人工智能(AI)与机器学习(ML)正以颠覆性力量,渗透药物从...
资源分享-202412-安徽药监-变更分类管理和具体实施(王彦忠)
文件是 2024 年 12 月 12 日 - 13 日安徽省药品监督管理局主办、中食药(天津)医药科技集团有限公司承办的全省药品生产质量管理现场培训班相关资料,核心围绕 GMP 变更管理展开,明确了变更的...




















kidzhangy5月前0
感谢分享,楼主好人一生平安Terrific6月前0
感谢!特别有用,资源分享的很及时!北岛2年前0
相当于货架期多久?Mark4年前2
Thanks for your blog, nice to read. Do not stop.一位WordPress评论者5年前0
嗨,这是一条评论。 要开始审核、编辑及删除评论,请访问仪表盘的“评论”页面。 评论者头像来自Gravatar。